- Предмети
- Резюме
- Передумови/цілі:
- Предмети/методи:
- Результати:
- Висновки:
- Вступ
- Предмети та методи
- Характеристика пацієнта
- Антропометрія
- Процедура трансплантації та визначення
- статистичні методи
- Результати
- Обговорення
Предмети
- Ожиріння
- Педіатрія
- Пересадка
Резюме
Передумови/цілі:
З'являється все більше доказів того, що стан харчування впливає на захворюваність та смертність дітей, які отримують лікування раку. Завдання цієї роботи - визначити, чи пов'язаний харчовий статус із виживаністю після трансплантації кісткового мозку після педіатрії.
Предмети/методи:
Це була ретроспективна одноцентрова ревізія пацієнтів, яким була проведена аутологічна або алогенна трансплантація гемопоетичних стовбурових клітин. Пацієнти були розділені на три вагові категорії: недостатня вага, ідеальна вага та надмірна вага, визначені у відсотках від ідеальної маси тіла. Результат, що цікавить, загальну виживаність після трансплантації, порівнювали між ваговими категоріями.
Результати:
З 113 пацієнтів 15 (13%) мали недостатню вагу, а 41 (36%) були класифіковані як надмірна вага. Після корекції віку, статі, джерела донора, кондиціонуючої терапії та року трансплантації пацієнти із надмірною вагою мали значно менше шансів вижити, ніж пацієнти з ідеальною вагою (коефіцієнт ризику (HR) 1,91; довірчий інтервал 95%, 1, 10-3, 31) . Не спостерігалося значного збільшення смертності при порівнянні пацієнтів із вагою із низькою вагою (HR 1,47; 95% довірчий інтервал, 0,57-3,79).
Висновки:
Діти із надмірною вагою до трансплантації гемопоетичних стовбурових клітин знизили рівень виживання порівняно з дітьми з ідеальною вагою.
Вступ
З'являється все більше доказів того, що стан харчування впливає на захворюваність та смертність у дітей, які отримують лікування раку; Отже, досягнення оптимального харчового статусу має велике значення як частина стандартної практики лікування. 1, 2, 3 Недавні результати досліджень показують, що практика клінічного харчування повинна не тільки обмежуватися запобіганням недоїданню, а й зменшувати частоту ожиріння у дітей з діагнозом лейкемія. 4, 5 Однак ці дослідження обмежуються харчовим статусом дітей при постановці діагнозу, і невідомо, чи впливає харчовий статус під час лікування, незважаючи на спостереження, що харчовий статус змінюється під час лікування. 6 Харчове втручання перед встановленням діагнозу неможливе, тому важливо направити дієтичне втручання на практичний момент часу під час терапії, наприклад, до трансплантації гемопоетичних стовбурових клітин (HSCT).
З огляду на можливий зв’язок між харчовим статусом та виживаністю у педіатричних хворих на ГСКТ та відсутність досліджень, які б досліджували цей взаємозв’язок, метою цього дослідження є дослідити зв’язок між харчовим статусом перед ХСКТ та виживанням у педіатричної популяції.
Предмети та методи
Характеристика пацієнта
Це було ретроспективне одноцентрове дослідження з червня 1998 р. По січень 2010 р. До дослідження були включені пацієнти, яким зробили аутологічну або алогенну трансплантацію в Королівській дитячій лікарні, Брисбен, Австралія з червня 1998 р. По січень 2007 р. За пацієнтами спостерігали не менше 3 років після трансплантації, оскільки попередні дослідження виявили, що криві виживання в цей час вирівнюються. 8,9 Королівська дитяча лікарня - третинний педіатричний центр для центральної та південно-східної частини Квінсленда та півночі Нового Південного Уельсу, який обслуговує 1,5 мільйона євро.
Дані для дослідження були отримані під час ретроспективного аудиту медичної картки. Дані включали вік, стать, зріст та вагу до HSCT, тип трансплантації та донора, початковий діагноз пацієнта та тип використовуваного кондиціонування. Результатом вимірювання було загальне виживання. Виживання визначали як час від початку підготовки до трансплантації до смерті. Протокол дослідження був затверджений Комітетом з етики Королівської дитячої лікарні.
Антропометрія
Пацієнти були розділені на три групи відповідно до% розрахованої ЧШТ: недостатня вага, ідеальна вага та надмірна вага. Вага та зріст були отримані за 9 днів до трансплантації. IBW визначали шляхом ідентифікації процентилю зросту пацієнта та вибору IBW за відповідним процентилем ваги, діаграми росту для дітей до 18 років, виготовлені Центрами контролю та профілактики захворювань, де вони використовувались. 13% IBW пацієнта розраховували шляхом ділення їх фактичної ваги на їх ідеальну вагу, метод, рекомендований Oncology Nutrition Dietetics Group, Американською дієтологічною асоціацією. 14 Порізи з недостатньою вагою, ідеальною вагою та надмірною вагою були взяті з Комітету з харчування дитячої онкологічної групи. 15 Одного пацієнта визначили як недостатню вагу, якщо його% IBW становив 110.
Процедура трансплантації та визначення
Процедури трансплантації класифікували за: (i) джерелом донора (аутологічне/пов'язане/не пов'язане); (ii) кондиціонуюча терапія (мієлоаблативна/немієлоаблативна); (iii) тип захворювання (злоякісне/не злоякісне). Джерело донорської терапії та кондиціонуюча терапія були пов’язані із суттєво різними результатами виживання, як і очікувалось. Для пацієнтів, яким була проведена багаторазова трансплантація, параметри трансплантації реєстрували при першій трансплантації.
Пацієнтів госпіталізували в окремі приміщення, провітрювані високоефективними системами фільтрації твердих частинок. Документована реактивація цитомегаловірусу або інфікування, показані за допомогою молекулярних ПЛР-тестів після трансплантації, лікували терапевтичними дозами фоскарнету або ганцикловіру. Пацієнти з ризиком рецидиву простого герпесу отримували профілактичний внутрішньовенний ацикловір. Емпіричні антибіотики широкого спектру дії та протигрибкова терапія при гарячці вводились згідно з інституційними протоколами. Після трансплантації пацієнти отримували профілактику котримоксазолу щодо Pneumocystis carinii. Протягом періоду дослідження використовувались різні препаративні схеми. Найпоширенішим із них є загальне опромінення тіла, яке вводять до дози 12 Гр протягом 3 днів по шість фракцій лінійним прискорювачем з подальшим циклофосфамідом 60 мг/кг на день протягом 2 днів або Бусульфаном 16 мг/кг загалом. перорально кожні 6 годин протягом 4 днів з подальшим введенням циклофосфаміду 50 мг/кг на день протягом 4 днів.
статистичні методи
За всіма пацієнтами, включеними у дослідження, спостерігали протягом принаймні 3 років після ІМТ або до смерті. Демографічні та клінічні характеристики порівнюються за допомогою тесту Манна-Уітні (безперервні дані) або точного тесту Фішера (категоріальні дані). Для оцінки різниці у виживаності між різними ваговими категоріями використовували регресійний аналіз пропорційних ризиків Кокса. Пацієнтів із надмірною та нижчою вагою порівнювали окремо з пацієнтами з ідеальною вагою. Спочатку ми розрахували некореговані коефіцієнти ризику (ЧСС) та 95% довірчих інтервалів, а потім розрахували скоригований показник ЧСС з урахуванням віку, статі, джерела донора, кондиціонуючої терапії та року трансплантації. Значимість була встановлена при P 0,05. Аналіз даних проводили за допомогою Stata 11.0 для Windows (Stata Corp., College Station, TX, США).
Результати
У досліджуваному періоді було 113 пацієнтів, які відповідали вимогам; 15 (12,6%) мали недостатню вагу, а 41 (34,5%) мали надлишкову вагу. Пацієнти мали широкий спектр злоякісних (n = 97) та не злоякісних (n = 16) діагнозів (табл. 1). Характеристики пацієнтів та трансплантатів наведені в таблиці 2. Групи із надмірною вагою та ідеальною вагою суттєво не відрізнялись. Однак, порівняно з групою ідеальної ваги, пацієнти з недостатньою вагою частіше були старшими (P = 0,0002), алогенними (P = 0,03), мали мієлоаблативний режим (P = 0,04) та мали додаткову хіміотерапію до загального опромінення тіла/Циклофосфамід (Флударабін, Тіотепа, Мелфалан або Етопозид ± АТГАМ-лімфоцитарний імуноглобулін, (АТГ-антитимоцитарний глобулін)) (Р = 0,03). Не було різниці у частці пацієнтів, які отримали загальне опромінення тіла за категоріями% IBW.
Повний розмір таблиці
Повний розмір таблиці
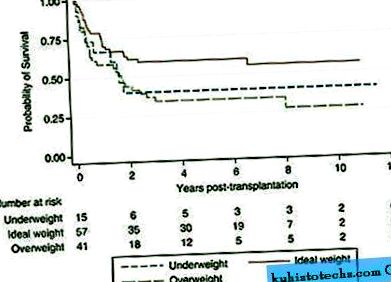
Медіана спостереження з дати трансплантації становила 6,9 року. Діапазон періодів спостереження за живими пацієнтами на кінець дослідження становив 3,1-11,5 років. На рисунку 1 показано рівень виживання за категоріями% IBW. Через 3 роки після HSCT 55 (49%) пацієнтів були живими; 6 (40%) у групі з низькою вагою, 34 (60%) у групі з ідеальною вагою та 15 (37%) у групі із зайвою вагою. Однофакторний показник HR для смертності суттєво збільшився у пацієнтів із надмірною вагою порівняно з пацієнтами з ідеальною вагою (HR; 95% довірчий інтервал = 1,97, 1,14-3,40) (таблиця 3). Ця асоціація зберігалася після коригування можливих незрозумілих змінних щодо віку, статі, джерела донора, кондиціонуючої терапії та року трансплантації. Істотних відмінностей у виживаності між категоріями з низькою та ідеальною вагою не було.
Графік виживання Каплана-Мейєра після трансплантації відповідно до категорії ідеальної маси тіла. Таблиця "Кількість ризику" показує кількість пацієнтів, які продовжують сприяти часу дослідження протягом кожного 2-річного інтервалу.
Повнорозмірне зображення
Повний розмір таблиці
Обговорення
Це дослідження показало, що діти з надмірною вагою, які перенесли аутологічний та алогенний HSCT, рідше виживають, ніж пацієнти з ідеальною вагою. Погіршення виживання у пацієнтів із надмірною вагою раніше спостерігалося у дітей із гострим лімфобластним лейкозом та гострим мієлоїдним лейкозом. 4, 5 Це стосується, зокрема, оскільки 23% пацієнтів, які отримують лікування гострого лімфобластного лейкозу, були визначені як ожиріння (% ІМТ 95%) наприкінці лікування. 6 Три дослідження з HSCT для дорослих показали, що ожиріння спричиняє зниження виживання в результаті збільшення смертності та рецидивів, пов'язаних з лікуванням. 16, 17, 18 Одне з цих досліджень включало підгрупу з 67 педіатричних пацієнтів і не виявило зв'язку між виживаністю та вагою. шістнадцять
Встановлено, що у дітей з вагою, що страждають лейкемією та солідними пухлинами, вищий рівень рецидивів та гірша виживаність. 3, 4, 21 Не було суттєвої різниці у виживаності між групами з низькою та ідеальною вагою. Хоча це і не суттєво, зростання ЧСС спостерігали з великими довірчими інтервалами, що вказує на необхідність подальших досліджень із більшими показниками у групі з низькою вагою. Група з недостатньою вагою суттєво відрізнялася від групи ідеальної ваги за віком, трансплантацією та типом кондиціонування. Трансплантація та тип кондиціонування контролювались; Однак віку не було. Група з низькою вагою була значно більшою, ніж ідеальна вага та групи із надмірною вагою. Однак це дослідження показало, що вік не робив істотного впливу на результат, тоді як Woolfrey et al. 9 виявили, що діти старше 10 років мали нижчі показники виживання без лейкемії та більшу частоту важких захворювань на трансплантат проти господаря та ускладнень, пов'язаних із схемою лікування після HSCT.
У цьому дослідженні% IBW використовувалось як показник харчового статусу,% IBW зазвичай використовується при оцінці харчування дитячих онкологічних хворих. Встановлено, що 2% IBW сильно і статистично значимо корелюють з ІМТ протягом багатьох періодів терапії дитячого раку, що робить його відповідним показником для вагових категорій. 15 відсотків IBW також можна використовувати для дітей 15, 22 Попередні дослідження, що аналізували стан харчування та виживання, використовували процентилі ІМТ та граничні значення, встановлені таблицями зростання Національного центру з контролю та профілактики захворювань від Національний центр статистики охорони здоров’я. 13
Це дослідження визначає надмірну вагу за допомогою антропометричних показників, а не за складом тіла; однак була виявлена сильна кореляція між відсотком жиру в тілі та% IBW у дитячій онкологічній популяції. 23 Пропонуються майбутні дослідження для вивчення впливу складу тіла на виживання хворих на рак, оскільки це може бути низький рівень маси клітин тіла (BCM) у пацієнтів із надмірною вагою, що призводить до поганого виживання. Попередні дослідження показали, що у дитячих онкологічних хворих може бути висока жирова маса, але низький рівень BCM. 24 Можливо, низька кількість BCM у пацієнтів із вагою та надмірною вагою пов’язана з виживаністю.
Це дослідження показало, що діти, які страждали надмірною вагою або страждали ожирінням до HSCT, частіше мали зниження виживання в порівнянні з ідеальною вагою у дітей. Причини цього не можуть бути визначені з цього дослідження; однак клінічні наслідки полягають у тому, що дієтологічне втручання повинно бути підходом для дітей із вагою та надмірною вагою до трансплантації кісткового мозку. Раніше недоїдання було центром підтримки харчування в дитячій онкології, і, як повідомляється, рівень недоїдання в деяких діагностичних категоріях досягав 50%. 25 Лікування ожиріння, як правило, не є частиною звичного управління клінічним харчуванням у пацієнтів дитячої онкології; однак цей документ базується на доказах того, що необхідна зміна клінічної практики. Зокрема, оскільки можливі втручання до ГСКТ, в цей час під час лікування можна застосовувати стратегії профілактики набору ваги та втрати ваги. Подальші дослідження повинні бути зосереджені на втручанні у харчуванні та фізичних вправах перед ТГСК та на впливі цього на поліпшення виживання.
- Надмірна вага є навіть більш смертоносним, ніж надмірна вага - Медичні новини - IntraMed
- Журнал способу життя Ожиріння та надмірна вага у дітей: передача від матері
- Адекватна дієта полегшує трансплантацію гемопоетичних стовбурових клітин; Іспанська асоціація
- Тайсон застосовував лікування стовбуровими клітинами для схуднення Esquire
- Втрата ваги нервової системи Надмірна вага PNG зображення - завантаження прозорого малюнка