Іспанська асоціація педіатрії має одним з головних завдань розповсюдження суворої та сучасної наукової інформації з різних областей педіатрії. Anales de Pediatría є Науковим висловлювальним органом Асоціації і є засобом, за допомогою якого співробітники спілкуються. У ньому публікуються оригінальні роботи з клінічних досліджень у педіатрії з Іспанії та країн Латинської Америки, а також оглядові статті, підготовлені найкращими професіоналами кожної спеціальності, щорічні повідомлення про конгрес та щоденники Асоціації, а також посібники для дій, підготовлені різними товариствами/спеціалізованими Секції, інтегровані в Іспанську асоціацію педіатрії. Журнал, орієнтир для іспаномовної педіатрії, індексується у найважливіших міжнародних базах даних: Index Medicus/Medline, EMBASE/Excerpta Medica та Index Médico Español.
Індексується у:
Index Medicus/Medline IBECS, IME, SCOPUS, Індекс наукового цитування розширений, Звіт про цитування журналів, Embase/Excerpta, Medica
Слідкуй за нами на:
Фактор впливу вимірює середню кількість цитат, отриманих за рік за твори, опубліковані у виданні протягом попередніх двох років.
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
Артеріальна протока - це структура, яка залишається відкритою під час внутрішньоутробного розвитку через ефект високого рівня простагландинів 1. Після народження рівень простагландину знижується, і природна тенденція протоки полягає у стихійному закритті в перші 3 дні життя. У недоношених дітей, особливо у тих, хто страждає на захворювання легенів, ці зміни відбуваються не однаково, і протока, ймовірно, залишатиметься відкритою після народження 2 (відкрита артеріальна протока [PDA]). Персистенція артеріальної протоки зі значним аортолегеневим шунтом може ускладнити еволюцію недоношених пацієнтів; спостерігалося підвищення стану ризику внутрішньошлуночкових кровотеч, некротизуючого ентероколіту, бронхолегеневої дисплазії та смерті 2-5. Захворюваність на КПК змінюється залежно від гестаційного віку та маси тіла при народженні, і чим вища, тим менша вага та вік вагітності; у недоношених дітей з дуже низькою вагою при синдромі респіраторного дистрессу він становить близько 40% на третій день життя 2,6,7. У нашому відділенні нинішня захворюваність на КПК становить 29% у осіб до 1500 г та зростає до 50% у тих, хто до 1000 г.
Індометацин, інгібітор синтезу простагландинів, був найбільш широко застосовуваним засобом для закриття КПК (або профілактично, або після діагностики) 2,4,5,8. Однак, незважаючи на доведену ефективність, його застосування було пов'язане з ускладненнями через зниження церебральної, ниркової та мезентеріальної перфузії 9-15 .
В останні роки з'явилися дослідження, які прийшли до висновку, що ібупрофен, ще один інгібітор синтезу простагландинів, був настільки ж ефективним при закритті КПК, але з меншим гемодинамічним ефектом 16-23, не обумовлюючи зменшення припливу крові до мозку, кишечника та нирок.
Тому було розроблено проспективне рандомізоване дослідження для порівняння ефективності та безпеки ібупрофену проти індометацину у недоношених дітей із симптоматичним АПД. Основною метою було закриття каналу після призначеного лікування, а вторинними - швидкість відкриття, необхідність другого раунду рятувального фармакологічного лікування, необхідність хірургічного закриття, частота ускладнень (некротизуючий ентероколіт, перфорація кишечника, ураження нирок, внутрішньошлуночкові крововиливи, інші крововиливи, бронхолегенева дисплазія) та смерть.
Пацієнт і методи
Вивчати дизайн
Перспективне клінічне випробування із випадковим розподілом та контрольною групою, яке було схвалено дослідницькою комісією та етичним комітетом нашого центру.
Дослідження проводилось у відділенні інтенсивної терапії Неонатологічної служби Університетської лікарні Ла-Фе у Валенсії (відділення III рівня, направлення до громади, на 16 ліжок та 460 щорічних прийому). Пацієнти були відібрані між січнем 2003 року та липнем 2004 року за попередньою інформованою згодою батьків.
Критеріями включення були недоношені діти з гестаційним віком менше 34 тижнів у перший тиждень життя, які мали PDA з гемодинамічно значущим шунтом, діагностували за допомогою ехокардіографії та потребували вентиляційної підтримки. Повне допплерівське ехокардіографічне дослідження (Hewlett Packard Sonos 2000 з датчиком 7,5 МГц) було проведено у всіх дітей педіатричними кардіологами з відділення новонароджених, враховуючи наявність домінантного аортолегеневого шунта із співвідношенням PDA/легеневий стовбур як гемодинамічно значущий шунт> 0,3 і зворотний діастолічний потік в черевній аорті 16,24 .
Ті пацієнти, у яких діурез був менше 1 мл/кг/год за 8 год до лікування, креатинін вище 1,8 мг/дл, тромбоцити менше 60000/мкл, активна кровотеча (трахеальна, травна або ниркова) були виключені нещодавно., периінтравентрикулярні крововиливи (3-4 ступеня) або важка гіпербілірубінемія.
Отримавши інформовану згоду батьків, пацієнти були рандомізовані на одне з двох втручань:
1. Індометацин (внутрішньовенна некислотна DAP MSD), 0,2 мг/кг/доза кожні 12 год, загалом 3 дози, що вводяться внутрішньовенною інфузією протягом 30 хв.
2. Ібупрофен (ібупрофен Orphan Europe®), який застосовували з початковою дозою 10 мг/кг, а потім 2 дозами 5 мг/кг кожні 24 год, шляхом внутрішньовенної інфузії протягом 20 хв.
Принаймні через 48 годин після початку цього першого циклу лікування був проведений ехокардіографічний контроль. Якщо протока залишалася відкритою і зі значним клінічним впливом, в якості порятунку вводили ще один раунд із 3 доз того самого препарату, спочатку призначеного. Якщо це друге лікування також не вдалося або його введення було протипоказано, і канал продовжував мати значні наслідки, ми переходили до хірургічного закриття.
Існування бронхолегеневої дисплазії визначали як потребу в додатковому кисні на 28 добу життя.
Функцію нирок оцінювали шляхом вимірювання рівня діурезу та рівня креатиніну протягом курсу лікування. Вважалося, що існувала минуща ниркова дисфункція (ТРЗ), коли спостерігалося зниження діурезу до 50% від базальної норми, але не досягаючи менш ніж 1 мл/кг/год або збільшення рівня креатиніну на 50% над базальним рівнем але менше 1,8 мг/дл. Перехідна ниркова недостатність (ТТІ) визначалася як зменшення діурезу нижче 1 мл/кг/год або підвищення рівня креатиніну вище 1,8 мг/дл.
Всім пацієнтам проводили лікування згідно з клінічними рекомендаціями та протоколами служби, а аналітичний та серцевий контроль, які вважалися адекватними, проводили до виписки з лікарні.
Розрахунок обсягу вибірки
Розрахунок обсягу вибірки базувався на головній залежній змінній дослідження. Відомо, що в популяції, подібній до нашої, частка спонтанних закриттів КПК становить 35%, а індометацин досягає 79% 4. Припускаючи частку 0,79 у контрольній групі (індометацин), приймаючи α-ризик 0,05 та β-ризик 0,20 у двосторонньому контрасті (статистична потужність 80%), та оцінюючи рівень втрат 5% подальшого спостереження, для виявлення різниці, що дорівнює або перевищує 40% між обома досліджуваними групами, необхідна загальна вибірка з 48 суб’єктів. Було використано наближення Arcsine, проведене за програмою Granmo 5.2 25 .
Для досягнення аналогічної кількості пацієнтів в обох групах послідовність рандомізації була сформована у двох групах із використанням процедури чотирьох елементів збалансованого блоку. Для використання функції "Випадкові" програми MS-Excel XP® була використана серія випадкових чисел, створених комп'ютером, і до цього застосована процедура, описана Фрідменом та ін. Після генерації послідовність рандомізації зберігалася прихованою, використовуючи техніку герметичного непрозорого конверта.
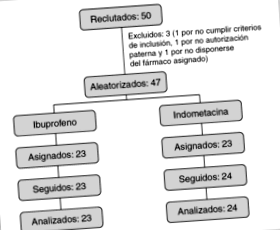
На рисунку 1 представлена блок-схема, на якій представлені пацієнти, які беруть участь у кожному з етапів дослідження.
Рисунок 1. Блок-схема учасників та подальші дії.
З 50 пацієнтів, які вважалися кандидатами на участь, троє були виключені до рандомізації: один через те, що батьки відмовились дати свою згоду; інший, оскільки він не відповідав одному з критеріїв включення (його післяпологовий вік перевищував 7 днів), і інший, оскільки, коли він збирався бути рандомізованим, було помічено, що одного з двох препаратів немає в аптеці обслуговування. Шанс нарешті розподілив 24 для лікування індометацином, а 23 - ібупрофену, і всі вони прослідковувались до кінця.
Таблиця 1 вказує, що рандомізація дала дві повністю порівнянні та взаємозамінні когорти в їх базових характеристиках до введення досліджуваного препарату.
Фармакологічне закриття каналу було досягнуто у 85,1% (точно 95% ДІ = 71,7-93,8) усіх недоношених дітей. Як видно з таблиці 2, частота закриття ліків була однаковою в обох когортах: 87,5% у групі, яка отримувала індометацин, і 82,6% у тій, яка отримувала ібупрофен (p = 0,7).
Також не було виявлено статистично значущих відмінностей між двома когортами щодо відновлення роботи після закриття, потреби у двох курсах прийому препарату або частки хірургічних перев'язок. З 9 пацієнтів, у яких фармакологічне закриття не було досягнуто, один помер, двоє не були перев’язані через відсутність клінічних чи гемодинамічних наслідків, а хірургічне перев’язування проведено у решти шести: двом у групі індометацину та чотирьом у групі ібупрофену.
Частота інших ускладнень була однаковою в обох групах (табл. 2). Жоден пацієнт, який отримував ібупрофен, не мав захворювання черевної порожнини, яке справді виявлялось у групі індометацину (дві перфорації кишечника та один некротизуючий ентероколіт). Сім пацієнтів (29%) у групі індометацину страждали TRD порівняно з двома (9%) у групі ібупрофену. У групі індометацину один розробив ІРТ, а жоден - у групі ібупрофену.
Жодна з двох когорт не мала вищої частоти бронхолегеневої дисплазії (30% індометацину проти 29% ібупрофену), важкого периінтравентрикулярного крововиливу (III-IV ступені) (4% у групі індометацину проти 9% у групі ібупрофену) або смертності (8,3 % проти 8,7%) (Таблиця 2). 4 померлих пацієнта мали масу тіла при народженні менше 750 г та термін вагітності менше 26 тижнів; помер на 5, 7, 9 та 131 день.
Так само не було виявлено статистично значущих відмінностей у тривалості штучної вентиляції легенів (p = 0,19), у тривалості додаткового надходження O 2 (p = 0,78) або у тривалості перебування у відділенні інтенсивної терапії новонароджених (NICU) ( р = 0,92).
Основною метою цього дослідження було визначити, чи ібупрофен, введений як значуще лікування кореневих каналів, діагностований у недоношених дітей на першому тижні життя, був таким же ефективним, як індометацин. У нашій серії обидва препарати виявились однаково ефективними при закритті симптоматичного КПК із швидкістю закриття, подібною до тієї, яка була виявлена в інших дослідженнях 16,17,21,28 .
Ібупрофен вже продемонстрував свою ефективність у закритті протоки у тварин 20,29. У людей мета-аналіз Кокрановського огляду 30 аналізує вісім досліджень, у тому числі в цілому 509 пацієнтів, що порівнюють ефективність ібупрофену проти індометацину при закритті протоки, і робить висновок, що жодне дослідження не виявляє суттєвих відмінностей в ефективності закриття КПК, ані мета -аналіз.
Зовсім недавно пропонувалося профілактичне використання ібупрофену 23,31 протягом перших годин життя, і проводяться випробування для оцінки його ефективності та безпеки при зменшенні захворюваності на КПК.
У нашому дослідженні не було доведено, що група, яка отримувала ібупрофен, мала більш високий ризик бронхолегеневої дисплазії, незважаючи на те, що частіше вимагав другого курсу лікування, хоча це спостерігалося в метааналізі Cochrane 2003, коли було проведено спільну оцінку двох досліджень. що окремо не показало суттєвих відмінностей 17,21,30. Різниця може полягати у частоті інших факторів, пов’язаних з дисплазією, або в невеликому розмірі нашої вибірки.
Також не виявлено істотних відмінностей у швидкості сильних внутрішньочерепних крововиливів. Тривала неврологічна еволюція не була оцінена, що було б дуже цікаво для майбутніх оглядів, оскільки експериментально спостерігався менший ефект ібупрофену на мозковий кровообіг та оксигенацію 18,22, з вигодами, які це могло б мати для нейророзвитку.
У жодного з наших пацієнтів не було епізодів гіпоксії, що свідчить про легеневу гіпертензію після введення ібупрофену, як описано Gournay та співавт. 38,39, які виявили 3 випадки легеневої гіпертензії після профілактичного введення ібупрофену недоношеним дітям віком до 28 тижнів. вагітність у перші 6 год життя. Причина цього ускладнення невідома і пов’язана з раннім введенням препарату, надзвичайною недоношеністю досліджуваної популяції та розведенням, що використовується для його використання (THAM, тришидроксиамінометан). У нашому аналізі як ібупрофен, так і індометацин розбавляли фізіологічним розчином або 5% сироваткою глюкози.
На закінчення в нашому дослідженні було показано, що ібупрофен є таким же ефективним, як індометацин, при закритті КПК. Не було суттєвих відмінностей у частоті ускладнень між цими двома групами, хоча у тих, хто отримував ібупрофен, було менше нирок та відсутність кишкових ускладнень. Зміни в еволюції дихання та виживанні не спостерігались. Було б зручно проводити нові дослідження, які б більш широко аналізували легеневі ускладнення та тривалу неврологічну еволюцію.
Ми хочемо висловити вдячність доктору В. Модесто за його співпрацю у статистичному аналізі дослідження.
- Лямблії у собак, зараження, симптоми та лікування - Блог Arion
- Натуральне маточне молочко з Італії, 10-денний цикл лікування
- 19-річна дівчина, яка відклала лікування, щоб доставити дитину, помирає від раку
- Las Cositas de EvaBeauty Моя думка щодо інтенсивного нічного лікування (Mercadona)
- Таким чином, передчасне старіння та вугрі впливають на забруднення шкіри