Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
Колумбійський журнал онкології є офіційним виданням Національного інституту раку (INC). Її періодичність щокварталу, а мета - розширити та поширити знання цієї медичної спеціальності. Журнал публікує статті про: молекулярні механізми канцерогенезу та відповідь на лікування; епідеміологія раку; клінічні характеристики та лікування пухлинних захворювань та заходи з охорони здоров'я для боротьби з раком.
Індексується у:
Scielo, DOAJ, Publindex, Imbiomed, Бузок, Latindex, Embase та ScienceDirect
Слідкуй за нами на:
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Рослинні сполуки, що застосовуються при лікуванні раку
- Механізми дії та хіміорезистентності
- Апоптоз та інгібуючі апоптоз білки
- Конфлікт інтересів
- Бібліографія
Натуральні продукти були найбільш репрезентативним джерелом отримання терапевтичних засобів для лікування раку, і їх величезний внесок визнано у відкритті нових цитотоксичних молекул з різними механізмами дії. Більшість препаратів, що застосовуються для лікування раку, не є дуже селективними та мають високий рівень стійкості та токсичності, що суттєво впливає на прогноз життя пацієнтів із цією хворобою. У цій статті розглядаються активні принципи, отримані з рослинних джерел для лікування раку, та їх різні механізми дії, розглядаючи найновіші досягнення в терапевтичних цілях, таких як білки, що інгібують апоптоз (IAP) та деякі структурно прості природні молекули, виявлені на різних фазах клінічного дослідження. дослідження, які цікаві на фармакологічному рівні завдяки своїй високій селективності, низькій токсичності та великому терапевтичному потенціалу проти різних типів раку.
Натуральні продукти були найбільш репрезентативним джерелом малих молекул для терапії раку і зробили величезний внесок у відкриття нових препаратів з різними механізмами дії. Більшість із цих препаратів є високотоксичними та мають низьку специфічність до ракових клітин, що суттєво впливає на прогноз виживання пацієнтів із цією хворобою. Метою даної статті є обговорення механізму дії біоактивних фітохімікатів проти раку. Представлені найбільш перспективні терапевтичні мішені, такі як інгібітор білків апоптозу (IAP), а також деякі біоактивні малі молекули, що мають фармакологічний інтерес та високу специфічність щодо ракових клітин.
Незважаючи на те, що в останні роки вчені відновили дослідження природних продуктів як джерела нових препаратів для лікування хронічних захворювань, таких як хвороба Альцгеймера, артрит, гепатит, діабет, туберкульоз, СНІД та рак; сьогодні багато країн, що розвиваються, продовжують використовувати традиційну медицину через низьку вартість та обмежений доступ до фармацевтичних методів лікування. Ці етноботанічні знання багато разів відповідають за відкриття нових активних принципів проти різних захворювань, наприклад, природні сполуки вінбластин, таксол, етопозид та іринотекан, серед багатьох інших, принесли нове світло для лікування хворих на рак 1 . Однак, хімічна та структурна складність, характерна для цих молекул, робить їх ізоляцію, структурне з'ясування та генерацію нових синтетичних шляхів важким та дорогим для отримання їх у більшій кількості.
Рослинні сполуки, що застосовуються при лікуванні раку
Важливість природних продуктів у розробці нових ліків полягає в тому, що 75% ліків, що використовувались для лікування раку та деяких інфекційних захворювань протягом 1981-2002 років, були отримані з натуральних продуктів; а пізніше, між 2002 і 2005 роками, завдяки природним джерелам на ринок було представлено 23 нові ліки для лікування різних захворювань 12. У 2007 та 2008 роках на ринок вийшло 55 нових препаратів, отриманих з природних продуктів, з яких 16 були виділені з природних джерел, а 39 отримані з хімічних структур, отриманих з них. Насправді, якщо із 206 препаратів, затверджених для лікування раку між 1940 і 2010 роками, виключити ті з високомолекулярними активними інгредієнтами, залишиться 175 препаратів, з яких 131 (приблизно 75%) пов’язаний з натуральними продуктами, або тому, що їх отримують безпосередньо з природного джерела, або отримують шляхом хімічного синтезу природної структури, або вносять невеликі хімічні модифікації до сполук, отриманих із природного джерела 14 .
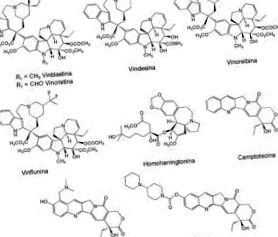
Серед природних рослинних сполук, які найбільше використовуються для лікування раку молочної залози, яєчок, легенів та лейкемії, є різні алкалоїди (рис. 1), такі як вінбластин та вінкристин, виділені з рослинних видів Catharanthus roseus (Apocynaceae), ендемічних для Мадагаскару п’ятнадцять; камптотецин, виділений із виду Camptotheca acuminata (Cornaceae) 16; і гомогаррінгтонін, виділений з вічнозеленого Cephalotaxus harringtonia K. Koch var. Гаррінгтонія (Cephalotaxaceae), яка походить з Японії. З цих сполук були розроблені напівсинтетичні похідні, які покращують їх активність або розчинність, такі як віндезин, винорелбін, вінфлунін, топотекан та іринотекан (рис. 1), останні два продаються як Hycamtin та Campostar від GlaxoSmithKline та Pfizer для товстої кишки та лікування раку яєчників 5,17 .
Протипухлинні алкалоїди в клінічному застосуванні, виділені з рослинних джерел (вінбластин, вінкристин, гомоаррінгтонін, камптотецин) та синтетичні аналоги (віндезин, винолербін, вінфлюнін, топотекан, іринотекан).
У сполуках типу лігнану (рис. 2) є нордигідрогуареатова кислота, виділена з виду Larrea tridentata (Zygophyllaceae) та подофіллотоксин, виділені з видів рослин роду Podophyllum (Berberidaceae), переважно Podophyllum peltatum та Podophyllum the notatum, з Отримані етопозидні та теніпозидні похідні, що використовуються для лікування різних типів лімфом та лейкозів 12. Також повідомляється про стильбени, такі як комбрестатини (рис. 2), виділені з рослинних видів Combretum caffrum (Combretaceae), де із комбстатину А 4 отримано аналог комбрестатину А 4-фосфату, який розчинний у воді і який показав, що Перспективна активність проти раку щитовидної залози в попередніх клінічних випробуваннях 18 .
Біоактивні фенольні сполуки проти різних типів раку. Типу лігнану (нордигідрогуареатова кислота, подофілотоксин, етопозид, теніпозид); стильбене (комбрестатин А4, комбрестатин А4Р) та флавоноїди (кверцетин, геністеїн, рохітукін, флавопіридол, феноксидіол, P276-00).
З'єднання флавоноїдного типу (рис. 2), які присутні в більшості зерен, овочів та фруктів, відіграють важливу роль у відкритті нових менш токсичних лікарських засобів завдяки їх захисному впливу на деякі типи раку; факт, який зробив їх потенційними агентами для лікування цієї хвороби 11. Хоча деякі флавоноїди почали оцінюватися в клінічних дослідженнях як профілактичні засоби, мабуть, найбільш вивченими для лікування деяких типів раку молочної залози, передміхурової залози та сечового міхура є кверцетин, геністеїн та рохітукін 9,19. Хімічні структури деяких флавоноїдів послужили відправною точкою для розробки терапевтичних засобів флавопіридолу, феноксидіолу та аналога Р276-00 (рис. 2), які виявляються в клінічних дослідженнях проти широкого спектра пухлин, включаючи лімфоми та лейкемії 20 .
Мабуть, найвідомішими хіміотерапевтичними засобами, отриманими з натуральних рослинних продуктів і використовуваними для лікування різних типів раку, є таксани 21–23 (рис. 3), представлені переважно паклітакселом, виділеним із рослинного виду Taxus brevifolia (Taxaceae) і спочатку відомим як таксол. З цієї хімічної структури було розпочато синтез доцетакселу та ортатакселу (рис. 3), які виявилися більш активними проти раку молочної залози, яєчників та легенів. Незважаючи на те, що в доклінічних дослідженнях 24,25 виявлено 23 різних таксани, і їх діяльність у лікуванні раку була дуже корисною, у сімействі Anonáceae повідомлялося про сполуки ацетогенінового типу, такі як булатацин (рис. 3), У 300 разів активніший, ніж таксол, при введенні мишам, які викликали пухлину з клітинами L-1210 (рак лейкемії). Миші, які отримували таксол, втратили 10% своєї ваги, тоді як ті, хто отримував булатацин, збільшили свою вагу на 5%, потенційно припускаючи, що він менш токсичний, ніж таксол. В даний час у різних клітинних лініях раку 26,27 вивчається понад 150 типів ацетогенінів .
Хіміотерапевтичні засоби, виділені з видів рослин родів Taxus (паклітаксел), Anonaceae (булатацин) та синтетичні аналоги (доцетаксел, ортатаксел).
Також повідомлялося про деякі сполуки ядра хінону (рис. 4), такі як β-лапафон, виділений з дерева лапачо Tabebuia avellanedae (Bignoniaceae), ембелін виду Embelia ribes (Myrsinaceae), що широко використовується в традиційній китайській медицині, і тимохінон 28 виду Nigella sativa (Ranunculaceae), які перебувають у різних фазах клінічного дослідження 29 для лікування деяких типів раку товстої кишки, яєчників, легенів, простати та молочної залози.
Протипухлинні сполуки на різних фазах клінічного дослідження, виділені з лікарських рослин. Тип хінону (β-лапахон, тимохінон, ембелін, іріасферин А, SAN5201); амід (піперин, піперлонгумін); Оксигенати (периліловий спирт, дилапіол, куркумін) та синтетичні аналоги (NSC295156, NSC698249).
Механізми дії та хіміорезистентності
Протипухлинні препарати, отримані з рослинних джерел, здебільшого характеризуються тим, що є антимітотичними агентами, які індукують загибель ракових клітин, як правило, коли вони перебувають у процесі мітозу 38. Це головна причина, чому вони також впливають на здорові клітини, викликаючи пошкодження будь-якої клітини в організмі, яка перебуває в процесі поділу, що породжує серію небажаних побічних ефектів у більшості хіміотерапевтичних процедур. Наприклад, камптотецин та його комерційні похідні Топотекан та Іринотекан діють на топоізомерази I та II, які є ферментами, що відповідають за вивільнення напружень, викликаних спіраллю ДНК під час її транскрипції, репарації та реплікації, роблячи регенерацію ДНК незворотною. пасмо після того, як її відокремили, щоб повторити або зняти напругу 39,40 .
Такі лігнани, як подофілотоксин та їх комерційні похідні Етопозид і Теніпозид, здійснюють свій механізм дії не лише впливаючи на топоізомеразу II, але також зв'язуючись з тубуліном, запобігаючи утворенню мікротрубочок і регенерації ДНК після його реплікації. Таксани, як подофілотоксин, діють на рівні мікротрубочок, але замість того, щоб перешкоджати їх утворенню в результаті полімеризації тубуліну, вони мають велику здатність стабілізувати свої структури і запобігати їх розчеплення, створюючи дисбаланс в клітині, що врешті закінчиться апоптозом 41 .
Інші сполуки, такі як ембелін, тимохінон та піперлонгумін, можуть діяти як антагоністи білків IAP 52, які відповідають за контроль каспаз, які є основними білками, відповідальними за виконання цієї форми запрограмованої загибелі клітин. Ці сполуки перешкоджають зв’язуванню білка XIAP з каспазами, звільняючи ефекторні каспази апоптозу, такі як каспази 3 і 7, запускаючи процес запрограмованої загибелі клітини в клітині. Наприклад, ембелін ефективний як окремо, так і в поєднанні з іншими препаратами на ракових клітинах, які виявляють надмірну експресію білка XIAP, у тому числі в клітинах PC-3 (рак передміхурової залози) 53 та в клітинах H460 (рак легенів) при застосуванні у комбінації з цисплатином, препарат, який широко використовується в хіміотерапії, до якої клітини H460 стійкі 54 .
Апоптоз та інгібуючі апоптоз білки
Апоптоз - це форма загибелі клітин, що характеризується різними морфологічними змінами, включаючи конденсацію хроматину, фрагментацію ядер, складки в плазматичній мембрані, розбирання цитоскелета та скорочення клітин. Ця форма запрограмованої загибелі клітин здійснюється каспазами, за допомогою яких клітина здійснює саморегульований внутрішній процес руйнування своїх білків, цитоскелета, органел, ядерної мембрани та ДНК, групуючи весь клітинний матеріал у невеликих тілах, що називається апоптотичні тіла, які згодом усуваються фагоцитозом, не викликаючи запального процесу 59. Цей процес запрограмованої загибелі клітин може бути активований загальним шляхом двома шляхами: внутрішнім і зовнішнім шляхом, які безпосередньо залежать від походження стимулу смерті 60 (рис. 5).
Шляхи активації апоптозу: Внутрішній шлях через мітохондрії, через вивільнення цитохрому С (Cit C), активацію каспази 9 (Casp. 9), утворення апоптосом і подальшу індукцію апоптозу через каспазу 3 (Casp. 3); зовнішній шлях через мембранні рецептори, пов'язані з доменами смерті FasL або TNF-R1, активація каспази 8 (Casp. 8) та подальша індукція апоптозу через каспазу 3.
- Наркотики До 12 годин ерекції через марихуани походження несподіваного пріапізму
- Кортикостероїди t; піки та вторинна надниркова недостатність; відносини; в тіні
- Придбайте овочевий смузі-протеїн Тонкий горох та коричневий рис Aquisana
- Придбайте Biogrowth Kokoh Bio Papilla (6 місяців) 400 г рослинної їжі Naturitas
- Купуйте органічне рослинне масло з розторопші 250 мл олії Terpenic Naturitas