REV CHIL OBSTET GINECOL 2012; 77 (2): 148 - 153
Документи
Передчасна недостатність яєчників: огляд
Каріна Хуарес Р. Доктор філософії 1a, Рікардо Лара А. PhD 1b, Хосе Гарсія О. PhD 1c
1 Відділ генетики, Centro de Investigación Biomédica de Occidente, CMNO-IMSS, Гвадалахара. Докторантура з генетики людини, Університет Гвадалахари; Гвадалахара, Халіско, Мексика.
біолог. b Фармацевт-біолог Хімік. c Медична.
Передчасна недостатність яєчників характеризується первинною або вторинною аменореєю, гіпоестрогенією та підвищеним рівнем ФСГ (фолікулостимулюючого гормону), що вражає 1 із 100 жінок у віці до 40 років. Етіологія його є багатофакторною. Лише у деяких пацієнтів може бути встановлена конкретна причина, зокрема: метаболічна, екологічна, аутоімунна, генетична та ятрогенна; будучи ідіопатичним близько 90% випадків. Серед генетичних причин можуть бути розглянуті зміни Х-хромосоми та мутації генів-кандидатів, які регулюють фолікулярний розвиток. Лікування повинно бути мультидисциплінарним, особливо зосередженим на замісній гормональній терапії та профілактиці ускладнень. Генетичне консультування важливо, щоб своєчасно приймати рішення, особливо у тих пацієнток, які все ще мають можливість завагітніти.
КЛЮЧОВІ СЛОВА: Передчасна недостатність яєчників, гени-кандидати, аменорея .
Передчасна недостатність яєчників характеризується первинною або вторинною аменореєю, гіпоестрогенією та підвищеним рівнем ФСГ (фолікулостимулюючого гормону), що вражає 1 із 100 жінок у віці до 40 років. Етіологія його є багатофакторною, однак лише у деяких пацієнтів може бути встановлена певна причина, включаючи: метаболічну, екологічну, аутоімунну, генетичну та ятрогенну, що є ідіопатичною у понад 90% випадків. Деякі з генетичних причин, які можна побачити, - це зміни Х-хромосом та мутації генів-кандидатів, які регулюють розвиток фолікулів. Лікування повинно бути мультидисциплінарним, зосереджуючись, зокрема, на замісній гормональній терапії та профілактиці ускладнень ранньої менопаузи. Генетичне консультування важливо для прийняття своєчасних рішень, особливо у тих пацієнтів, які все ще мають шанс завагітніти.
КЛЮЧОВІ СЛОВА: Передчасна недостатність яєчників, гени-кандидати, аменорея .
ВСТУП
Передчасна недостатність яєчників (POI), також відома як передчасна недостатність яєчників або передчасна менопауза, визначається як припинення
Овуляція та ендокринні функції яєчників у жінок віком до 40 років. Цей термін був вперше запропонований у 1942 році Фуллером Олбрайтом, який вважається батьком ендокринології (1,2).
Це стан, який, за оцінками, вражає 1 із 100 жінок у віці до 40 років (1%), 1 із 1000, які не досягли 30 років (0,1%), і 1 з 10 000 жінок, які не досягли 40 років. 20 років (0,01%) (3,4). Однак було описано, що відповідно до етнічного походження показники можуть змінюватися: 1,4% для афро-американських та латиноамериканських жінок, 1,0% для кавказьких жінок, 0,5% для китайських та 0,1% для японських жінок (5).
З іншого боку, підраховано, що для жінок з первинною аменореєю (відсутність першої менархе) її поширеність становить 10-28%, а для жінок з вторинною аменореєю (зміна менструального циклу) вона становить 4-18% (6, 7,8).
Завдання цього огляду - надати загальний та поточний огляд ВГД, що дозволяє краще зрозуміти та правильно керувати клінічною практикою.
КЛАСИФІКАЦІЯ
З клінічної точки зору POI можна розділити на спорадичні форми (переважна більшість випадків) та сімейні форми, де ризик рецидивів оцінюється до 33%, підтверджуючи, що POI є спадковим станом. (9.10) . Що стосується спорадичних випадків, повідомляється, що близько 50% пацієнток могли відновити функцію яєчників навіть після встановлення діагнозу, що призвело до несподіваних вагітностей у 5-15% (11,12).
За наявністю або відсутністю фолікулів в яєчнику ВГД можна класифікувати на дві різні гістопатологічні групи: афолікулярну та фолікулярну. При афолікулярній формі відбувається повне виснаження фолікулів яєчників і, отже, постійна втрата функції яєчників; З іншого боку, у фолікулярній формі можна знайти фолікули в яєчнику, хоча можуть відбуватися патологічні процеси, що перешкоджають його нормальній функції; Однак в останньому стані існує можливість повернення до функції яєчників як спонтанно, так і індуковано (13,14).
ДІАГНОСТИКА
У більшості жінок вік першої менархе та менструальний цикл є нормальними (15); однак наявність первинної або вторинної аменореї може слугувати орієнтиром для встановлення діагнозу POI (7,16). Епідеміологічні дослідження показали, що середній вік, в якому діагностується POI, становить 33,5 ± 4,8 року, із середнім віком появи симптомів 25 років (17).
В даний час не існує уніфікованих діагностичних критеріїв POI, хоча більшість клініцистів вважають, що такий стан виникає при аменореї протягом 3 місяців і більше, коли рівні ФСГ перевищують 40 мМО/мл і якщо рівні естрадіолу менше 50 пг/мл, значення Що необхідно вимірювати принаймні два рази в різні місяці, оскільки рівні можуть коливатися (3,15,18).
В рамках клінічної історії пацієнтів з POI зручно досліджувати сімейний анамнез, попередні операції на яєчниках, опромінення, аутоімунні захворювання, стани, які стосуються Х-хромосоми або інших генетичних захворювань (5). Діагноз POI може бути підтверджений лабораторними дослідженнями, які включають: β-hCG (β-хоріонічний гонадотропін людини), LH (лютеїнізуючий гормон), FSH, пролактин та естрадіол. Важливо проводити каріотип жінки і в ідеалі проводити молекулярні дослідження (5,15,19).
ЛІКУВАННЯ
Найбільшим ризиком, пов'язаним з ВГД, є дефіцит естрогену, який впливає на мінеральну щільність кісток, що призводить до остеопорозу, крім серцево-судинних та неврологічних захворювань, таких як хвороба Альцгеймера (12, 20, 21); однак безпліддя залишається найбільш руйнівним побічним ефектом у пацієнтів з ІР (22).
Враховуючи, що діагностика POI може впливати як на фізичне, так і на емоційне здоров'я, лікування повинно бути мультидисциплінарним (12). Гіпоестрогенним жінкам потрібно вжити заходів проти остеопорозу, тому вони повинні включати кальцій і вітамін D у свій раціон, не нехтуючи фізичними вправами, крім того, щоб уникати таких факторів ризику, як споживання тютюну та алкоголю (15). З іншого боку, замісна гормональна терапія (ЗГТ) зменшила ризик серцево-судинних захворювань, остеопорозу, а також підтримку статевої функції (23). Симптоми менопаузи, такі як припливи, нічне потовиділення та сухість піхви, контролювалися за допомогою прийому протизаплідних таблеток (15,20).
Таким чином та через відсутність методів лікування, які відновлюють роботу яєчників, одним із найбільш часто використовуваних варіантів сприяння вагітності є донорство яйцеклітин. Очікується, що найближчим часом стане можливим дозрівання ооцитів, отриманих із стовбурових клітин, in vitro, а також збереження тканин яєчників (20,23). У випадку молодих жінок, які пройдуть хіміо- або променеву терапію, рекомендується кріоконсервація ооцитів (11).
Що стосується ведення пацієнтів з POI та враховуючи, що в останні десятиліття тенденція до народження дітей у більш пізньому віці значно зросла, було б доцільним, щоб у випадках, коли є сімейний анамнез POI, слід наполягати на ранньому діагнозі, а також адекватне генетичне консультування, яке дозволяє досягти паритету в більш ранньому віці або вибрати репродуктивні альтернативи в клініках із допоміжною фертильністю (21).
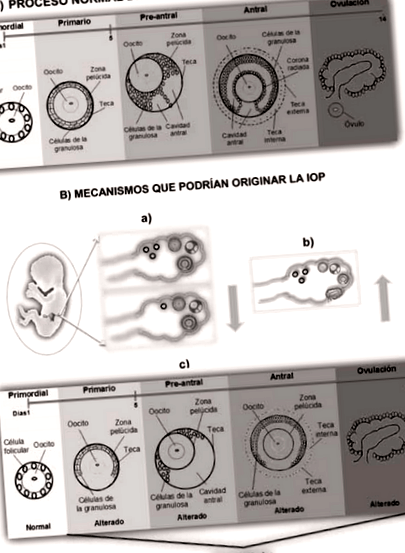
Хоча причина POI невідома в більшості випадків (90%) (13), припускають, що такий стан може бути обумовлений наступними механізмами: а) зменшенням початкової кількості фолікулів, б) прискореною фолікулярною атрезією або с ), що відбувається зміна процесів дозрівання фолікулів (22,24) (рис. 1).
| Фігура 1. А) Нормальний процес дозрівання фолікулів людини. Б) Можливі механізми, що спричиняють передчасну відмову яєчників (POI): а) початкове зменшення кількості фолікулів, б) прискорена фолікулярна атрезія та в) зміна процесів дозрівання фолікулів. |
Такі механізми можуть активуватися з різних причин, включаючи ятрогенні (хіміотерапія або променева терапія), метаболічні, інфекційні, токсичні, екологічні, аутоімунні та генетичні фактори (4,25,26). Що стосується взаємозв'язку між аутоімунітетом та POI, то було підраховано, що 10-30% дорослих пацієнтів з цим станом будуть мати аутоімунне захворювання, включаючи гіпоадреналізм, гіпотиреоз, міастенію та системний червоний вовчак, і хоча є повідомлення, які підтверджують наявність анти-яєчникових антитіл у сироватці крові пацієнтів з POI, взаємозв'язок між ними досі залишається суперечливим, а точні механізми незрозумілі (11,15).
Широко було продемонстровано генетичну участь у POI, прикладом чого є моносомія X-хромосоми при синдромі Тернера, яка вважається найпоширенішою хромосомною зміною, пов’язаною з POI (27). Інші зміни, такі як делеції, транслокації, інверсії та дублювання в одній і тій же хромосомі, дозволили ідентифікувати критичні ділянки (Xp11.1 - Xp21, POF1: Xq21.3-q27 і POF2: Xq13.3-q21.1), що містять важливі гени для функції яєчників, які були пов’язані з ВГД (28, 29, 30).
Делеції терміналів, що відбуваються в області Xp11, можуть спричинити як випадки первинної аменореї, так і ВГД. Делеції, що залучають довге плече Х-хромосоми, як правило, призводять до ВГД, хоча можуть бути деякі винятки. Фенотип, асоційований з проксимальною делецією Xq13, включає первинну аменорею, відсутність теларху, гіпергонадотропний гіпогонадизм і повну недостатність яєчників. Коли область Xq21 бере участь у делеції, тоді підтримка функції яєчників порушена, де, за підрахунками, існує вісім різних генів, відповідальних за розвиток яєчників. Делеції, що походять з регіону Xq25 або q26, призведуть до вторинної аменореї (29,31,32).
Що стосується участі аутосомних генів, було описано, що область 5q14.1-q15 містить гени, експресовані в яєчнику, і що вони можуть брати участь у ВГД (22); однак, хоча лише невелика кількість мутацій була пов'язана з ВГД (FMR1, FMR2, AIRE, FSHR, LHR, GALT1, BMP15, FOXL2, EIF2B, NOGGIN, POLG та INHA), все ще існує велика кількість генів-кандидатів (DIAPH2, DFFRX, WT1, 2FX, ATM, XIST), розташовані в критичних для ВГД областях, або які втручаються на певній стадії розвитку фолікулів, або від утворення первинних фолікулів, до передовуляційних фолікулів, які можна було б проаналізувати до пояснити випадки, коли певна причина не була виявлена (ідіопатична) (8,9,29,33). У таблиці I представлений список генів-кандидатів з найбільшою участю в етіології POI.
POI - гетерогенна та багатофакторна хвороба, яка впливає як на фізичне, так і на психологічне здоров’я молодих жінок, тому надзвичайно важливо співпраця мультидисциплінарної групи, яка надає адекватні поради та подальші заходи як у випадках з афолікулярними POI, так і в ті, у кого ще є певний резерв яєчників і у кого є можливість досягти вагітності.
ЛІТЕРАТУРА
1. Купер А.Р., Бейкер В.Л., Стерлінг Е.В., Райан М.Є., Вудрафф Т.К., Нельсон Л.М. Настав час нового підходу до первинної недостатності яєчників. Фертил Стерил 2010; 95: 1890-7. [Посилання]
2. Pal L, Santoro N. Передчасна недостатність яєчників (POF): розбіжність між соматичним та репродуктивним старінням. Aging Res Rev 2002; 1: 413-23. [Посилання]
3. Maclaran K, Horner E, Panay N. Передчасна недостатність яєчників: тривалі наслідки. Менопауза Int 2010; 16: 38-41. [Посилання]
4. Jagarlamudi K, Reddy P, Adhikari D, Liu K. Генетично модифіковані моделі мишей для передчасної недостатності яєчників (POF). Ендокринол Mol Cell 2010; 315: 1-10. [Посилання]
5. Nippita T, Baber R. Передчасна недостатність яєчників: огляд. Climacteric 2007; 10: 11-22. [Посилання]
6. Ляо С, Фу Ф, Ян Х, Сун Я.М., Лі ДЗ. Аналіз китайських жінок з первинною недостатністю яєчників методом порівняльної геномної гібридизації з масивом із високим дозволом. Чін Мед Дж (англ.) 2011; 124: 1739-42. [Посилання]
7. De-Vos M, Devroey P, Fauser BC. Первинна недостатність яєчників. Lancet 2010; 376: 911-21. [Посилання]
8. Сузуморі Н., Пангас С.А., Райкович А. Гени-кандидати передчасної недостатності яєчників. Curr Med Chem 2007; 14: 353-7. [Посилання]
9. Діксіт Н, Рао Л, Падмалатха В, Расесварі Т, Кумар А, Панда Б. Гени, що регулюють передчасну недостатність яєчників. Reprod Biomed Online 2010; 20: 724-40. [Посилання]
10. Ni F, Wen Q, Wang B, Zhou S, Wang J, Mu Y, Ma X, Cao Y. Мутаційний аналіз гена FOXL2 у китайських пацієнтів з передчасною недостатністю яєчників. Гінеколь Ендокринол 2010; 26: 246-9. [Посилання]
11. Vujovic S, Brincat M, Erel T, Gambacciani M, Lambrinoudaki, Moen MH. Заява про позицію EMAS: Управління жінками з передчасною недостатністю яєчників. Maturitas 2010; 67: 91-3. [Посилання]
12. Калу Е, Панай Н. Спонтанна передчасна недостатність яєчників: проблеми управління. Гінеколь Ендокринол 2008; 24: 273-9. [Посилання]
13. Нельсон Л. Клінічна практика: Первинна недостатність яєчників. N Engl J Med 2009; 360: 606-14. [Посилання]
14. Sinha P, Kuruba N. Передчасна недостатність яєчників. J Obstet Gynaecol 2007; 27: 16-9. [Посилання]
15. Обстріли АН. Передчасна недостатність яєчників. Розмноження 2010; 140: 633-41. [Посилання]
16. Massin N, Czernichow C, Thibaud E, Kuttenn F, Polak M, Touraine P. Ідіопатична передчасна недостатність яєчників у 63 молодих жінок. Horm Res 2006; 65: 89-95. [Посилання]
17. Кулам CB, Адамсон, SC, Annegers JF. Захворюваність на передчасну недостатність яєчників. Obstet Gynecol 67: 604-10. [Посилання]
18. Ferreira S, Matoso E, Pinto M, Almeida J, Liehr T, Melo J, Carreira I. Делеція Х-хромосомного терміналу у жінки з передчасною недостатністю яєчників: Гаплонедостатність Х-зчеплених генів як можливе пояснення. Mol Cytogenet 2010; 3: 14. [Посилання]
19. Фаснахт З, Мемпель А, Стровіцкі Т, Фогт П.Х. Синдром передчасної яєчникової недостатності (POF): до молекулярно-клінічного аналізу його генетичної складності. Curr Med Chem 2006; 13: 1397-410. [Посилання]
20. Cartwright B, Robinson J, Rymer J. Лікування передчасного дослідження недостатності яєчників: опис триваючого клінічного дослідження. Менопауза Int 2010; 16: 18-22. [Посилання]
21. Бек-Пеккоз П., Персані Л. Передчасна недостатність яєчників. Orphanet J Rare Dis 2006; 1: 9. [Посилання]
22. Persani L, Rossetti R, Cacciatore C. Гени, що беруть участь у передчасній недостатності яєчників у людини. J Mol Endocrinol 2010; 45: 257-79. [Посилання]
23. Панай Н, Фентон А. Передчасна недостатність яєчників: зростаюче занепокоєння. Climacteric 2008; 11: 1-3. [Посилання]
24. Woad KJ, Watkins WJ, Prendergast D, Shelling AN. Генетична основа передчасної недостатності яєчників. Aust N Z J Obstet Gynaecol 2006; 46: 242-4. [Посилання]
25. Asbagh FA, Ebrahimi M. Повідомлення про випадки спонтанної вагітності під час гормональної замісної терапії передчасної недостатності яєчників. Іранський J Reprod Med 2010; 9: 47-9. [Посилання]
26. Мандон-Пепін Б, Турен П, Куттен Ф, Дербуа С, Руксель А, Мацуда Ж. Генетичне дослідження чотирьох мейотичних генів у жінок з передчасною недостатністю яєчників. Eur J Endocrinol 2008; 158: 107-15. [Посилання]
27. Cameron M, Grover S, Moore P, Jayasinghe Y. Нехромосомна, не ятрогенна передчасна недостатність яєчників у підліткової популяції: серія випадків. J Pediatr Adolesc Gynecol 2008; 21 (1): 3-8. [Посилання]
28. Вуйович С. Етіологія передчасної недостатності яєчників. Менопауза Int 2009; 15: 72-5. [Посилання]
29. Сімпсон JL. Генетична та фенотипова неоднорідність у оглядовій недостатності огляду відібраних генів-кандидатів. Ann N And Acad Sci 2008; 1135: 146-54. [Посилання]
30. Welt CK. Первинна недостатність яєчників: більш точний термін для передчасної недостатності яєчників. Clin Endocrinol (Oxf) 2008; 68: 499-509. [Посилання]
31. Сімпсон Дж. Л., Райкович А. Диференціація яєчників та недостатність статевих залоз. Am J Med Genet 1999; 89: 186-200. [Посилання]
32. Бонді С, Нельсон Л, Калантаріду С. Генетичне походження недостатності яєчників. J Womens Health 1998; 7: 1225-9. [Посилання]
33. Ceylaner G, Altinkaya S, Mollamahmutoglu L, Ceylaner S. Генетичні відхилення у турецьких жінок з передчасною недостатністю яєчників. Int J Gynaecol Obstet 2010; 110: 122-4. [Посилання]
34. Тіотіу Б, Меркадал А, Імберт Р, Вербіст Дж, Деместер І, Де Лінер А. Варіанти гена BMP15 у когорти пацієнтів з передчасною недостатністю яєчників. Hum Reprod 2010; 25: 1581-7. [Посилання]
35. Laissue P, Vinci G, Veitia R, Fellous M. Недавні досягнення у вивченні генів, що беруть участь у несиндромічній передчасній недостатності яєчників. Ендокринол Mol Cell 2008; 282: 101-11. [Посилання]
36. Wang J, Liu J, Zhang Q. Мутації FOXL2 у китайських пацієнтів із синдромом блефарофімосіптозу епікантус інверсус. Mol Vis 2007; 13: 108-13. [Посилання]
37. McIntosh C, Lun S, Lawrence S, Western A, McNatty K, Juengel J. Прорегіон миші BMP15 регулює кооперативні взаємодії BMP15 та GDF9. Biol Reprod 2008; 79: 889-96. [Посилання]
38. Laml T, Preyer O, Umek W, Hengstschlager M, Hanzal H. Генетичні порушення при передчасній недостатності яєчників. Оновлення Hum Reprod 2002; 8: 483-91. [Посилання]
39. Fan QR, Hendrickson WA. Будова гормону, стимулюючого фолікули людини, в комплексі з його рецептором. Nature 2005; 433: 269-77. [Посилання]
40. Лівшиць Г., Підлісна С, Кравченко С, Судома І, Лівшиць Л. Розподіл двох SNP в екзоні 10 гена FSHR серед жінок зі зменшеним запасом яєчників в Україні. J Assist Reprod Genet 2009; 26: 29-34. [Посилання]
Весь вміст цього журналу, крім випадків, коли він ідентифікований, підпадає під ліцензію Creative Commons
Роман Діас # 205, Депто. 205, Провіденсія
Тел .: (56-2) 22350133
Факс: (56-2) 22351294