- предметів
- реферат
- вступ
- Вікова дегенерація жовтої плями
- Β - розширення, структура та динамічна збірка
- Механізми дії β у дегенеративних нейронах
- Докази Aβ у старінні сітківки та ВМД
- Формування конститутивного Aβ в нормальній сітківці
- Навантаження сітківки на сітківку Ap збільшується з віком
- Агрегація стор бере участь у ключових стадіях AMD
- P- відкладення сітківки провокують прозапальні та проангіогенні мікросередовища
- Фактори ризику AMD сприяють розвитку А β агрегація в старінні сітківки
- Тваринні моделі лікування ВМД та анти-Аβ антитілами
- Β та AMD - уроки нейродегенерації та подальших дій
предметів
реферат
Вікова дегенерація жовтої плями (ВМД) - це складний очний розлад, що вражає критичну ділянку сітківки, відомий як макула, що є критичним для центрального зору та сприйняття дрібних деталей. Хвороба є основною причиною незворотної сліпоти в суспільствах, демографічні показники яких сприяють збільшенню віку. Етіологія цього дегенеративного розладу маловідома, але включає як генетичні, так і фактори ризику навколишнього середовища. 1, 2, 3 Основним фактором дегенеративної патології є втрата зорової функції, пов'язана з атрофією фоторецепторів та основним пігментним епітелієм сітківки (RPE), який утворює гемато-ретинальний бар'єр. 4, 5 Гангліозні клітини сітківки (RGC) та моношар RPE нещодавно були визначені головним джерелом синтезу та секреції амілоїдного бета (Aβ) у задньому оці. 6 Aβ - це високопроникний і високотоксичний білок, який агресивно націлений на нейрони і є ключовою особливістю нейродегенеративних захворювань. 7, 8 Більше резервуарів Aβ було виявлено в оці в середовищі сітківки, тоді як підвищений рівень Aβ був виявлений у старінні сітківки та пов'язаний з ключовими стадіями прогресування ВМД. 6 Ці висновки підтверджують гіпотезу про те, що Aβ відіграє вирішальну, хоча і нехарактерну раніше роль, в русі дегенеративних процесів у старінні макули.
Тут ми збираємо найновіші знання з літератури, що вивчає ВМД, нейродегенерацію, а також β-структурну біологію, що підтверджує нашу гіпотезу, та надаємо уявлення про основні дегенеративні події, які можуть погіршити старіння сітківки. Краще розуміння того, як Aβ може націлюватись на функцію сітківки, може допомогти у розробці нових методів лікування ВМД у майбутньому.
Вікова дегенерація жовтої плями
ВМД є найпоширенішою причиною незворотної сліпоти в суспільствах, що старіють, і позначається на глобальному рівні
50 мільйонів осіб, прямі витрати яких оцінюються у майже 255 мільярдів доларів. 9 Хвороба вражає
Хоча ВМД була клінічно охарактеризована, основні механізми, особливо під час раннього перебігу захворювання, залишаються не повністю відомими. Отже, відсутність молекулярної характеристики сухої та вологої ВМД обмежило наше розуміння та визначення захворювання переважно клінічними спостереженнями та термінологією. Недавнє відкриття Aβ у старіючій сітківці та її асоціація з ВМД представляє цікаву можливість поглянути на ВМД з нової точки зору та краще зрозуміти початок та прогресування захворювання за допомогою нових молекулярних термінів.
Β - розширення, структура та динамічна збірка
Ген білка-попередника амілоїду (APP), розташований у хромосомі 21q21, кодує повсюдно експресований інтегральний мембранний глікопротеїн типу I у декількох альтернативних сплайсингових формах, найпоширеніші ізоформи яких включають APP 751, APP 770 та APP 695. Як повідомляється, транскрипти APP та білки експресуються рясно в мишах, щурах, а також у клітинах RGC та RPE людини, 14, 15, причому APP 695 є основною ізоформою, що експресується в мозку. 16 Функції APP залишаються неповними, і більшість досліджень пропонують передачу сигналів через кілька шляхів у мозку. 17 Протеолітична обробка APP відбувається двома взаємовиключними шляхами, які називаються амілоїдогенними та неамілоїдогенними (або конститутивними) шляхами. 18, 19 Поступове розщеплення АРР амілоїдогенним шляхом ферментами β- та γ-секретази продукує мономерний Aβ-пептид з молекулярною масою
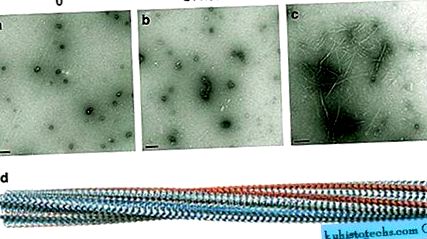
(a - c) Перегляньте негативно забарвлені електронні мікрофотографії, що демонструють самостійне збирання Aβ 1-42 при рН 7, 4, 50 μ M. (a) Показує невеликі сферичні олігомери, які видно відразу після приготування пептиду Aβ 1-42. (Soura et al. 50). Потім вони збираються протягом 24 годин, щоб утворити (b) подовжені протофібрили і, нарешті, (c) амілоїдні фібрили після 48 годин інкубації. d Показує структурну модель амілоїдного волокна, що складається із структури ß і демонструє повільну скручену архітектуру. Генерація моделей описана в Morris et al. 101
Повнорозмірне зображення
Механізми дії β у дегенеративних нейронах
Докази Aβ у старінні сітківки та ВМД
Формування конститутивного Aβ в нормальній сітківці
І сітківка, і центральна нервова система (ЦНС) мають спільне походження, оскільки обидва походять від нервової трубки, що розвивається. Обидві структури тісно пов'язані з сусідньою судинною системою через гемато-сітківковий та гематоенцефалічний бар'єри. Зі збільшенням віку як на сітківці, так і в головному мозку з’являються позаклітинні відкладення, пов’язані з дегенеративною патологією, іменовані друзами та старечими бляшками. Тому не дивно, що багато вражаючих подібностей між друзами та старечими бляшками включають Aβ. Інші спільні компоненти включають наступне; компонент амілоїду Р сироватки крові, аполіпопротеїн Е, імуноглобулін, матриці базальної мембрани, протеоглікани та іони металів (Fe 3+, Cu 2+ та Zn 2+), реагенти гострої фази, елементи, пов’язані з протеазою/кліренсом, та кілька доповнюючих білків, а також як інші медіатори запалення, які припускають місцеве запалення, як правило, пов’язане з відкладеннями сітківки. Така дивовижна схожість між друзами та старечими бляшками, що узгоджується з віком та поганим клінічним прогнозом, свідчить про те, що подібні патологічні механізми можуть призвести до дегенеративних змін як сітківки ока, так і мозку.
Діафрагма сітківки сітківки збільшується з віком
Осадження Ss із збільшенням віку не обмежувалось лише суб-RPE-регіонами, але несподівано виявилося, що воно накопичується у зовнішніх сегментах фоторецептора (POS) у літніх мишей. Такі відкладення були виявлені лише через 3 місяці, а через 12 місяців зовнішні сегменти були повністю обгорнуті A-вмісним матеріалом, який виявився якісно різним протягом 24 місяців. 60 Хоча немає прямих доказів того, що такий матеріал є чистим Aβ, тісний зв'язок між імунозабарвлюючими Aβ-схемами та скануванням EM-зображень стверджує, що Aβ є принаймні елементом таких вікових відкладень. Крім того, інтравітреальне введення олігомерного Aβ40 щурам дикого типу виробляло найвищий рівень інтенсивності імунозабарвлення в POS, підтримуючи ідею переважного накопичення Aβ в апікальній близькості клітин RPE. Аналіз посмертних зразків людини у віці від 31 до 90 років відображає подібну закономірність збільшення імунофарбування β у POS. Ця модель накопичення Aβ, яка починається з апікального піку POS і продовжує свою довжину, ілюструє специфічну агрегацію Aβ, 60, і як така узгоджується з іншими висновками 14, 54, 55, 56, які показують Aβ сітківку/RPE накопичення. у задньому оці з похилим віком (рис.2).
Схема, що показує кілька ділянок синтезу, секреції та агрегації Aβ у старіючій сітківці (червона зірочка), про що повідомляється в літературі. BrM, мембрана Бруха; POS, зовнішні сегменти фоторецептора; RGC, гангліозні клітини сітківки; RPE, пігментний епітелій сітківки.
Повнорозмірне зображення
Агрегація p бере участь у ключових стадіях AMD
Aβ-групи переважають у осіб із середнім та високим рівнем друзів. Aβ розміщений у сферичних структурах, які називаються «амілоїдними пухирцями», які можуть займати значну частину друзу та створювати потенційні ділянки активації комплементу. Друз може бути щільно упакований у кілька амілоїдних пухирців або може містити лише одну велику везикулу. Наявність різних Aβ-структур може відображати еволюційний характер трутнів із прогресуванням захворювання. Наприклад, наявність декількох олігомерних ядер у великій друзі може бути зумовлена меншою агломерацією друнтів з часом. Ap у друзе корелює з дегенеруючими фоторецепторами та RPE. CC, хоріокапіляріс; BrM, мембрана Бруха; RPE, пігментний епітелій сітківки.
Повнорозмірне зображення
Р-відкладення в сітківці викликають прозапальні та проангіогенні мікросередовища
Фактори ризику AMD сприяють агрегації β у старінні сітківки
Тваринні моделі лікування ВМД та анти-Аβ антитілами
Як вікове дегенеративне захворювання зі складною етіологією відтворення повного спектру патології ВМД на моделях тварин. Однак це не завадило розробити багато тваринних моделей гризунів, кроликів, свиней та приматів, що не є людьми. Широко використовувані моделі мишей/щурів мають перевагу у нижчій вартості, простоті обслуговування та здатності розвивати симптоми захворювання за відносно короткий проміжок часу, але страждають від дефектів, більшість з яких включають відблиски - це недостатність жовтої плями. Критично важливо, що жодна модель не мала успіху у відтворенні повного спектру захворювань ВМД, хоча існують переконливі моделі, що відтворюють обмежені особливості як географічної, так і ексудативної форм захворювання. На відміну від цього, використання приматів, що не є людиною, дає можливість вивчати ВМД у системі, яка має більш схожість та фізіологію з людьми, але має ряд недоліків, включаючи значні етичні наслідки, проблеми генетичних маніпуляцій та більш тривалі часові шкали. до початку захворювання.
Β та AMD - уроки нейродегенерації та подальші кроки
Тут ми обговорили гіпотезу та нові захоплюючі висновки, які показують, що Аβ здатний відігравати ключову роль у ВМД, вивчення яких може запропонувати краще розуміння механізмів раннього захворювання, а також молекулярних шляхів, що підтримують хронічну сітківку. дегенерація. Приклади спільної патології у хворих на АД включають зменшену товщину нервового волокна, 99 аномальне кровообіг сітківки 62, а також зменшену товщину судинної оболонки, 100 ділянок, де дегенерація також відбувається при глаукомі та ВМД. 1, 5, 74 Подібні особливості виявляються також між старечими бляшками AD та друзом AMD6, а також характер селективного пошкодження тканин, що свідчить про спільні молекулярні механізми принаймні на деяких стадіях цих захворювань. Дослідження Aβ та пов'язаної з ними патології сітківки можуть запропонувати нові перспективи щодо ВМД та підійти до цієї виснажливої сліпучої хвороби з нової точки зору. Такі дослідження вже проводяться в нашій лабораторії.