Цей повний текст є відредагованою та переглянутою стенограмою лекції, проведеної в рамках клінічних зустрічей Педіатричної служби Оздоровчого комплексу Сан-Борха-Арріарбн. Публікація цих наукових звітів стала можливою завдяки редакційній співпраці Medwave та Педіатричної служби. Керівником служби є д-р Франциско Баррера, а координатором клінічних зустрічей - д-р Луїс Дельпіано.
Церебральний параліч (ХП) - це складне захворювання, яке може проявлятися по-різному і з різним ступенем ураження. Пацієнти з неврологічними пошкодженнями займають у деякі періоди року близько 30% ліжок у педіатричній службі лікарні Сан-Борха-Арріарбн; їх середні дні госпіталізації довші, ніж у дітей без неврологічних пошкоджень, насправді частина цих пацієнтів практично мешкає в лікарні, і їх госпіталізація, як правило, дорожча, оскільки їм часто потрібні ліки або лабораторні дослідження та візуалізація більшої складності, особливо молочні суміші, інфузійні насоси, догляд та респіраторна або рухова терапія. Поліпшення харчового статусу хворих на ХП зменшує частоту госпіталізацій та інфекцій та покращує якість їхнього життя та якості їхніх сімей чи осіб, що виховують.
Проблемами харчування, які мають діти з ХП, є:
- недоїдання;
- недостатність росту (довжина);
- надмірна вага або ожиріння;
- дефіцит мікроелементів або через недостатнє споживання та/або через певну взаємодію між ліками та поживними речовинами, що перешкоджає правильному метаболізму;
- остеопенія та остеопороз;
- Труднощі з проведенням адекватної оцінки харчування як для діагностики, так і для подальшого спостереження.
Є ряд факторів, які сприяють розвитку харчових змін у дітей із ХП, серед них: грубі та дрібні моторні зміни; порушення ковтання та рухова дисфункція ротової порожнини; гастроезофагеальний рефлюкс, викликаючи аспірації, вторинні респіраторні інфекції та недостатнє споживання їжі через гіперемезіс; відсутність амбулаторії; залежність від опікунів, які не завжди підходять; сенсорні порушення; кісткові деформації хребта та грудної клітки, які ускладнюють дренування бронхіального секрету, введення їжі та догляд за пролежнями; час еволюції: чим довший час еволюції неврологічного компромісу, тим більший харчовий компроміс; споживання їжі, яка часто є недостатньою через вищезазначені розлади; використання зондів для годування або гастростом; вживання ліків, особливо протисудомних, які шкідливо впливають на щільність кісток; навчання в сестринській допомозі в лікарнях, установах або вдома; нарешті, є фактор витрат, оскільки багато разів вихователь повинен кидати роботу, щоб піклуватися про дитину.
У дослідженні, яке було проведено для оцінки труднощів у харчуванні групи дітей з ХП, у яких спостерігалася недостатність росту як за тривалістю, збільшенням ваги, так і за дефіцитом якості життя, автори провели антропометрію та класифікували труднощі для годування за наявністю порушень ковтання, рухових порушень, порушень постави, неврологічних пошкоджень, помітного зниження активності, наявності запорів та ступеня затримки спорожнення шлунка. Вони також застосували опитування якості життя вихователя (1). У цьому дослідженні було помічено, що збільшені труднощі у годуванні цих дітей пов'язані з більшими змінами в лінійному зростанні та прирості ваги, меншим запасом жиру, вимірюваним складками трицепсів, більшою кількістю госпіталізацій, більшою частотою респіраторних інфекцій та гіршою якістю життя опікунів (рис. 1).
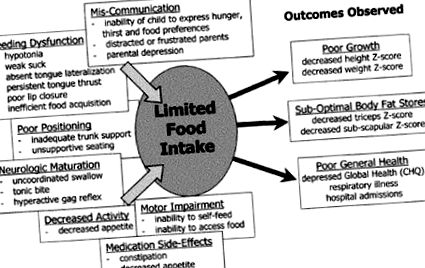 |
| Фігура 1. Порушення функції харчування, зростання та стан здоров’я у дітей з ХП. |
Метою управління харчуванням у дітей з ХП є досягнення адекватного стану харчування, що дозволяє підтримувати такі функції: кардіореспіраторну, за допомогою адекватного тонусу діафрагмальної та серцевої мускулатури; імунологічний, для боротьби з інфекцією; рухові та когнітивні через адекватне функціонування неврологічної системи; загоєння та відновлення тканин, щоб уникнути пролежнів або дозволити їм швидко розсмоктатися. Ці цілі досягаються, якщо крива вага-зріст (P/T) підтримується на 10-му процентилі (p10) системи NCHS, у випадках важкого ХП.
Оцінка харчування дитини з ХП включає:
- Віддалений та поточний анамнез, з якого можна визначити час еволюції.
- Оцінка кривої зростання.
- Спостерігайте за актом годування та труднощами, що виникають під час нього: ступінь самодостатності, рухові розлади, ковтання, наявність рефлюксу, постави, сколіоз, тривалість, кашель тощо.
- Оцініть споживання.
- Вкажіть вживання наркотиків та отримайте опис сімейно-соціальної мережі підтримки.
Фізичний огляд повинен оцінити рухову активність та м’язовий тонус. Нарешті, слід провести антропометрію, враховуючи, що важко зважити цих дітей, оскільки багато разів вони не можуть встати, а антропометричні оцінювальні крісла не завжди доступні; Крім ваги, необхідно вимірювати довжину або зріст; окружність голови, хоча це не є хорошим параметром для подальшого спостереження; окружність рук і складки, з них складчастість трицепсів є найбільш представницькою за складом тіла.
Діти з ХП мають інший характер зростання, ніж звичайні діти, через їх різний склад тіла, зі зниженою щільністю кісткової маси, м’язової маси, жирової маси та лінійним ростом, а також закономірності розвитку пубертату та віку кісток. У 2007 році були опубліковані таблиці для оцінки росту дітей та підлітків із ХП на основі багатоцентрових досліджень, які включали 24 920 дітей та підлітків віком від 2 до 20 років, в яких було проведено 141 961 вимірювання ваги та зросту (2). Автори класифікували хворих на ХП на п’ять груп за групою моторикою:
- Група 1: ходіть поодинці, не менше шести метрів і добре балансуйте.
- Група 2: ходіть з підтримкою або нестабільністю мінімум три метри.
- 3 група: повзе або повзе, але не ходить.
- 4 група: прострація, не може прогодуватися, але не має гастростомії.
- Група 5: рухові характеристики групи 4, але вона харчується гастростомою. Факт наявності гастростомії покращує харчовий статус і, отже, лінійний ріст.
Згадані таблиці наведені на рис. 2. Один зліва відповідає співвідношенню вага/вік у жінок; суцільна лінія відповідає певним дітям із ХП, а пунктирна лінія - NCHS. Видно, що 10-й процентиль відрізняється, а не 90-й процентиль, в якому обидві криві схожі, оскільки ці діти вже здатні ходити. Таблиця праворуч відповідає групі 5, тобто нічним дітям, які харчуються гастростомою; пунктирна лінія відповідає NCHS, а суцільна - новій. Помічено, що 10-й процентиль лінії NCHS відповідає 90-му процентилю нової кривої, тобто тип зростання, який вони досягають, дуже різний, як за вагою/віком, так і за зростом/віком (2, 3). У групі 4, які не використовують гастростому і яка не відображається на цьому графіку, крива ще менша (рис. 2).
| Малюнок 2. Схема зростання серед популяції дітей та підлітків із ХП. |
Діти з ХП часто страждають від скутості та гіпертонусу, тому їх потрібно вимірювати за сегментами та вимірювати у порівнянні з таблицями, що використовуються в даний час, які були опубліковані в 1995 році та були підготовлені на основі невеликої групи із 170 дітей та лише 211 вимірювань. довжина гомілки, що дозволяє отримати загальну довжину за формулою (4). На жаль, ці таблиці корисні лише до 12 років (рис. 3).
| Малюнок 3. Вимірювання довжини гомілки для обчислення загальної довжини у дітей з ХП. |
Існує кілька методів виявлення недоїдання у дітей з ХП. У часто цитованому дослідженні Фанг та його колеги визначали недоїдання як відсоток площі плечового жиру менше 5% для віку та статі в таблицях дітей без неврологічних пошкоджень (5). Вони виміряли вагу, зріст і складки і дійшли висновку, що складний трицепс р10 найкращий інструмент для скринінг ніж співвідношення Р/Т, завдяки своїй високій чутливості, для оцінки недоїдання, визначеного як низький р5 в жировій ділянці окружності надпліччя відповідно до статі та віку (зменшений жировий запас), у дітей з ХП (табл. I).
| Таблиця I. Виявлення недоїдання у дітей з ХП: погана корисність Р/Т. |
Корисні лабораторні параметри для оцінки поживності включають:
- червоний ряд для виключення анемії
- альбумінемія
- азот сечовини, який може бути на низькому рівні через зменшення споживання або зменшення м’язової маси
- фосфемія, лужні фосфатази, вітамін D та денситометрія кісток для оцінки кісткової маси
- відеофлюороскопія для дослідження ковтання
- 24-годинний рН-метр для дослідження рефлюксу
- оксиметрія під час годування та
- Цілодобова креатинінурія, яка служить показником м’язової маси та запасу білка.
У дослідженні, в якому вимірювали преальбумінемію та альбумінемію у 107 дітей із середньою та важкою ХП, з метою оцінки ступеня недоїдання на основі альбумінемії, було виявлено, що більшість пацієнтів мали більш високий рівень альбуміну від 3,5 до 3,9 і навіть вище 4 г/дл, незважаючи на те, що він має -4 стандартні відхилення у співвідношенні Р/Е; лише 8% мали рівень альбуміну менше 3,5 (6). Отже, рівень альбуміну в плазмі не відображає харчовий статус у дітей із ХП (Таблиця II).
| Таблиця II. Концентрація преальбуміну та сироваткового альбуміну не відображає харчовий статус у дітей із ХП. |
Таблиці, що співвідносять цілодобову креатинурію та зріст, були опубліковані в 1981 році, але вони базувались на людях без неврологічних пошкоджень (7). Оскільки креатинін - це м’язовий білок, для оцінки кількості м’язової маси у дитини можна розрахувати відсоток нормального креатиніну, що виділяється кожним пацієнтом. Опис нормальних значень для дітей з ХП в літературі не зустрічається (Таблиця III).
| Таблиця III. Індекс креатинінурії 24 год/висота. Вимірювання м’язового білка. |
Потреби в енергії можна розрахувати за різними формулами.Важливо, що згодом відстежують вагу та зріст, щоб оцінити, чи є внесок адекватним; мета - досягти P/T на 10-му процентилі NCHS. Вживання білка слід приймати, дотримуючись рекомендацій для звичайних дітей, а також споживання мінералів та вітамінів. Було помічено, що навіть коли дітям із ХП дають добавку, вони все ще мають дефіцит заліза, фолієвої кислоти, ніацину, кальцію та вітаміну Е і D, і що ентеральне споживання покращує рівень цих мікроелементів у плазмі крові (8).
Потреба в енергії розраховується за допомогою рівняння, яке забезпечує загальну енергію, помножуючи основні витрати енергії на м’язовий тонус та рівень активності, до якого додається очікуваний нормальний ріст. М'язовому тонусу присвоюється значення 1, якщо це нормально, 0,9, якщо у нього гіпотонія, і 1,1, якщо дитина гіпертонічна (9). Потреба в енергії, як правило, набагато нижча за норму, оскільки у цих пацієнтів змінений склад тіла та крива росту, а їх активність значно нижча, ніж у здорової дитини.
У таблиці IV показано взаємодію між ліками та метаболізмом мікроелементів: антациди, антагоністи Н2, інгібітори протонної помпи та антиконвульсанти втручаються в цей метаболізм, отже, пацієнти, які використовують фенітоїн або фенобарбітал, повинні отримувати добавки вітаміну D. а ті, хто лікується вальпроєвою кислотою, карнітином.
| Таблиця IV. Взаємодія між ліками та поживними речовинами: фактор метаболізму мікроелементів. |
Введення годування дітям із ХП може здійснюватися перорально, чого багато матерів досягають, змінюючи консистенцію їжі. Альтернативою є ентеральний шлях за допомогою назогастрального або назоєюнального зонда або гастростомії; може бути болюсно або безперервно (загальний або нічний), і може знадобитися додавання препаратів для лікування рефлюксу та/або запору.
У пацієнтів з неврологічною патологією ентеральне харчування слід розглядати з урахуванням одного або декількох з наступних факторів: неможливість приймати 80% необхідної кількості через рот; загальний час годування більше чотирьох годин на день; пацієнт віком до двох років з недостатнім зростанням або збільшенням ваги більше місяця; пацієнт старше двох років із втратою ваги або без збільшення ваги протягом трьох місяців; зміна у двох вигнутих каналах росту (P/E або P/T), або стійкі незначні складки трицепса p5. Якщо ці ситуації зберігаються більше місяця, слід розглянути питання про гастростомію.
Кістковий метаболізм дітей з ХП характеризується високою поширеністю остеопенії, що пов'язано зі ступенем недоїдання; насправді, найбільш прогностичним фактором остеопенії є помітний компроміс кривої Р/Е. Іншими факторами, які сприяють цьому явищу, є: вік (чим старша кістка, тим менша щільність кістки), тяжкість неврологічного пошкодження, труднощі з годуванням, історія попереднього перелому та використання протисудомних препаратів, які викликають остеопенію багаторазовим механізми: порушення обміну кальцію, гіпофосфатемія, підвищений вміст лужних фосфатаз, підвищений рівень ПТГ, зниження рівня активного вітаміну D, рентгенологічні дані рахіту та гістологічні дані остеомаляції (10).
