Дієтолог-дієтолог (AND-00980); Кандидат біологічних наук та сільськогосподарських харчових наук, Кордовський університет
Вступ
Серед варіантів встановлення успішного протоколу щодо надмірної ваги та ожиріння ми маємо вказати дієту з високим вмістом білка (ЛП), яка, як було показано, є ефективною у забезпеченні більш ситного ефекту (1) та допомозі у схудненні (2). Здається, механізм цього відбувається в шлунково-кишковому тракті, де білок можна виявити, модулюючи механізми регуляції апетиту (3).
Крім того, прийом протоколу НР щодо прийому їжі матиме вплив на: i) підвищений термогенез, ii) кишковий глюконеогенез та iii) зміни гормонального профілю кишечника (4).
Вищезазначені механізми можуть бути наслідком присутності амінокислот внаслідок перетравлення білка. Відомо, що різні типи білків можуть мати рівень насичення, можливо, через різний склад амінокислот (АА). Амінокислоти можна виявити в кишечнику, щоб сприяти викиду кишкових гормонів з аноректичним ефектом. Наприклад, ароматичні АА l-фенілаланін і l-триптофан індукують вивільнення холецистокініну (CCK), а інші гормони, такі як глюкагоноподібний пептид (GLP-1) та пептид YY (PYY), виділяються у відповідь на наявність поживних речовин. ., серед них АА (5).
Ці гормони діють безпосередньо на ділянки мозку, які беруть участь у регуляції апетиту. CCK, грелін, PYY та GLP-1 впливають на апетит та споживання їжі (6).
Здатність L-аргініну стимулювати вивільнення GLP-1 та PYY вивчали in vitro (7). L-аргінін - це умовно незамінна амінокислота, що отримується з дієти, ендогенного синтезу та обміну білків.
Вважається, що кожен АА забезпечує певний фізіологічний сигнал про контроль прийому їжі. На наступному графіку ми отримали результат через 12 годин без їжі у гризунів при вживанні їжі відповідно до типу введеного АА (8).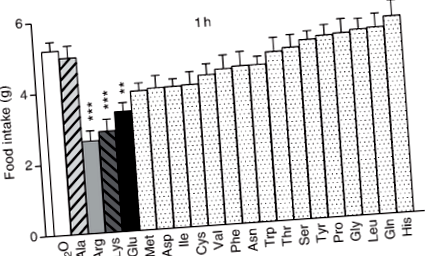
Мета цього допису - краще зрозуміти, як АА L-аргінін може допомогти нам у протоколі, орієнтованому на лікування ожиріння.
Вплив на пероральне введення L-аргініну на споживання їжі, масу тіла та витрати енергії у гризунів
Як у щурів, так і у мишей, пероральне введення L-аргініну призвело до зниження споживання їжі як натщесерце рано вранці, так і в умовах ad libitum пізно вдень (9)
Додамо, що ні у щурів, ні у мишей зміни витрат енергії після цього тесту не виявлені.
Анорексичні властивості L-аргініну
Дози, виявлені в дослідженнях на гризунах, мають фармакологічний рівень, і кількість, яка може еквівалентна харчуванню з 45% білка. Однак цей хронічно підтримуваний протокол не передбачає зменшення ваги після постійного повторення початкової дози. У цьому сенсі для встановлення стратегії періодів та доз у середньо- чи довгостроковій перспективі при застосуванні L-аргініну бракує досліджень, які можуть допомогти дослідити його потенціал у боротьбі з ожирінням.
L-аргінін, L-лізин та L-глутамінова кислота
Поряд з L-аргініном, іншими 2 АА, визначеними з найвищим анорексичним потенціалом, є L-лізин та L-глутамінова кислота (8).
Ці 3 АА викликають розтягнення шлунка, затримуючи спорожнення шлунка. Існують механізми, за допомогою яких певні АА регулюють травлення та харчову поведінку.
Для підтримки гомеостазу поживних речовин центральна нервова система інтегрує сигнали, що стимулюють або гальмують дію їжі. Постачання необхідних АА регулюється шляхом регулювання споживання їжі відповідно до вмісту білка в їжі, тобто існує система виявлення АА на індивідуальному рівні, яка дозволяє шляхом передачі певних сигналів контролювати споживання їжі (розуміти один одного, Багато моментів, коли ми голодні, цей сигнал може бути наслідком відсутності деяких важливих АА. Наше враження може бути "я голодний", але якщо цього не станеться, ми пропонуємо продукти, що забезпечують ці АА, незабаром після цього ми будьте знову голодними. Цю ситуацію легко впізнати професіоналам, які проходять консультації з питань харчування).
Із 20 АА, що існують, внесок згаданих 3 передбачав велике зменшення споживання їжі. Пояснення цьому міститься у впливі цих 3 АА на нейрональну активність в області постеми та ядра одиночного тракту (аспекти, в яких ми не будемо вникати далі в цій публікації).
Графік, який би пояснив анорексичний потенціал аргініну, лізину та глутаміну.
L-аргінін та резистентність до інсуліну
L-аргінін є попередником оксиду азоту.
Серед супутніх захворювань з найбільшим впливом ожиріння є інсулінорезистентність. Синдром інсулінорезистентності (IRS) схильний до діабету 2 типу, серцево-судинних захворювань, гіпертонії, деяких видів раку, синдрому полікістозних яєчників, жирової печінки та апное сну.
У пацієнтів із серцево-судинними захворюваннями (ССЗ) дисфункція ендотелію існує в морфологічно інтактних судинах ще до появи клінічних проявів при ССЗ. Добре встановлено, що знижена біодоступність оксиду азоту (NO) сприяє дисфункції ендотелію.
Активація NO-синтази (NOS) збільшує кровотік та чутливість до інсуліну в тканинах (наприклад, скелетних м’язах, печінці та жировій тканині). Інгібування NOS зменшує надходження поживних речовин на мікросудинному рівні та спричиняє вузьке місце або притуплення в скелетних м'язах поглинання глюкози, стимульоване інсуліном.
Згадаймо, що синтез NO судинним ендотелієм регулює артеріальний артеріальний тиск (10) і є дефектним у пацієнтів з гіпертонічною хворобою (11).
Утворення оксиду азоту
Резюме
У пошуках створення ефективних протоколів для осіб із надмірною вагою або ожирінням, знання механізму дії певних амінокислот може допомогти у розробці більш ефективних дієт.
(1) P oppitt SD, McCormack D, Buffenstein R. Короткотермінові ефекти попереднього навантаження макроелементів на апетит та споживання енергії у худорлявих жінок. Фізіол Бехав 1998; 64: 279–285
(2) Westerterp-Plantenga MS, Lejeune MP, Nijs I, van Ooijen M, Kovacs EM. Високе споживання білка підтримує підтримку ваги після втрати ваги тіла у людей. Int J Obes Relat Metab Disord 2004; 28: 57-64
(3) Fromentin G, Darcel N, Chaumontet C, Marsset-Baglieri A, Nadkarni N, Tome D. Periferni та центральні механізми, що беруть участь у контролі надходження їжі харчовими амінокислотами та білками. Nutr Res Rev 20 12; 25: 29–39.
(4) Halton TL, Hu FB. Вплив дієт з високим вмістом білка на термогенез, ситість і втрату ваги: критичний огляд. J Am Coll Nutr 2004; 23: 373–385
(5) Spreckley E, Murphy KG. L-клітина у харчовому зондуванні та регуляції апетиту. Передня гайка 20 15; 2:23
(6) Бертуд HR. V-агальний та гормональний зв’язок кишечник-мозок: від насичення до задоволення. Neurogastroenterol Motil 2008; 20 (Додаток 1): 64–72.
(7) Mace OJ, Schindler M, P atel S. Регуляція активності K- та L-клітин за допомогою GLUT2 та кальцій-чутливого рецептора CasR у тонкому кишечнику щурів. J Physiol 20 12; 590 (Pt 12): 29 17–2936.
(8) Jordi J, Herzog B, Camargo SM, Boyle CN, Lutz TA, V errey F. Specic амінокислоти інгібують споживання їжі через десертну область або аферентні ділянки вагуса. J Physiol 20 13; 59 1 (Pt 22): 56 1 1–562 1.
(9) А. Аламшах, A .K .M c G a v i g a n, Е. Шпреклі та ін. L-аргінін сприяє викиду гормонів кишечника та зменшує споживання їжі у гризунів. Діабет, ожиріння та метаболізм 18: 508–518, 2016.
(10) Шеселі Е.Г., Маеда Н, Кім Х.С. та ін. Підвищений артеріальний тиск у мишей, у яких відсутня ендотеліальна синтаза оксиду азоту. Proc Natl Acad Sci U S A 1996; 93: 13176–81
(11) Forte P, Copland M, Smith LM, Milne E, Sutherland J, Benjamin N. Базальний синтез оксиду азоту при есенціальній гіпертензії. Lancet 1997; 349: 837-42
