Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
Іспанська хірургія є офіційним органом Іспанської асоціації хірургів (AEC) та Іспанського товариства торакальної хірургії (SECT), обидва наукові товариства охоплюють більшість загальних та грудних хірургів, а також інші субспеціальності іспанської хірургії. Журнал є найкращим показником технічного та концептуального розвитку іспанської хірургії таким чином, що на його сторінках, подібно до еволюції, яку пережила хірургія у світі, все більше уваги приділяється біологічним та клінічним аспектам хірургічної патології, перевищуючи таким чином оперативну дію, яка в минулому була головним акцентом уваги в цій галузі медицини. Зміст журналу структуровано за розділами «Оригінали», «Огляди», «Клінічні примітки» та «Листи до редактора», а статті відібрані та опубліковані після ретельного аналізу відповідно до міжнародних стандартів.
Індексується у:
SCIE/JCR, Index Medicus/Medline, IBECS, IME
Слідкуй за нами на:
Фактор впливу вимірює середню кількість цитат, отриманих за рік за твори, опубліковані у виданні протягом попередніх двох років.
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
Внутрішньопротокова муцинозна папілярна пухлина підшлункової залози (IMTT) приділяється особлива увага в останні роки завдяки зростаючій частоті та різному клінічному та патологічному прояву 1-3. Всесвітня організація охорони здоров’я визначає його як внутрішньопротокове новоутворення, що продукує муцин, яке бере свій початок у головному протоці (TPMI-CD) або його гілках (TPMI-R). TPMI було розділено на 4 категорії за ступенем клітинної атипії: а) аденома; б) невизначений (кордон); в) карцинома in situ, і г) інвазивна карцинома. Частота інвазивної карциноми коливається від 25 до 45%.
Найчастіша клінічна картина 3 - при болях у животі (49-82%), гострому панкреатиті (13-64%) та втраті ваги (29-50%). Інші клінічні відхилення включають раптовий початок цукрового діабету (11-72%), жовтяницю (9-18%) та екзокринну недостатність (7-17%).
Незалежно від того, чи є у них інвазивна карцинома, це є найважливішим фактором прогнозу у цих пацієнтів з TPMI, тому всі пухлини, незалежно від їх розміру, повинні бути піддані патологічному дослідженню. Хірургічне втручання повинно бути першим варіантом лікування цих пацієнтів через складність розмежування інвазивних та неінвазивних форм TPMI 4 .
IMTD-CD є дифузним ураженням підшлункової залози і вимагає від широкої панкреатектомії до повної панкреатектомії. TPMI-R, як правило, асоціюється з меншими пухлинами і з меншою ймовірністю інвазивного злоякісного ураження, ніж TPMI-CD, переважне розташування якого знаходиться в голові підшлункової залози, особливо в області нецинованого процесу. Кефалічна панкреатикодуоденектомія типу Уіппла або з пілоричним збереженням є найбільш часто використовуваною методикою 5,6. Однак ці характеристики TPMI-R дозволять лікувати це новоутворення за допомогою консервативної хірургічної операції. Останні включають часткову резекцію головки підшлункової залози із збереженням дванадцятипалої кишки (техніка Бегера 7), часткову резекцію головки підшлункової залози з видаленням вентральної підшлункової залози та дванадцятипалої кишки (техніка Pedrazzoli et al. 8), а також тотальну резекцію головки підшлункової залози з сегментарна дуоденектомія (методика Nakao 9). Ці методики повинні зберегти адекватну васкуляризацію на різних рівнях дванадцятипалої кишки та жовчної протоки, щоб вони могли мати ішемічні ускладнення.
Метою даної роботи є оцінка результатів консервативної хірургії дванадцятипалої кишки у пацієнтів з TPMI-R. Також аналізуються результати втручання Уіппла у пацієнтів з TPMI.
Пацієнти та метод
З січня 1995 р. По січень 2006 р. 34 пацієнти (20 чоловіків та 14 жінок) були оперовані ТПМІ середнім віком 65 років (діапазон 48-78 років). Хвороба локалізована у 21 пацієнта (14 чоловіків та 7 жінок) в голові підшлункової залози; у 7 пацієнтів, в тілі хвоста підшлункової залози, а у 6 пацієнтів також була кістозна пухлина в голові підшлункової залози і дифузна дилатація протоки Вірсунга.
Група аналізу в цій роботі відповідає підгрупі з 21 пацієнта з пухлинами, розташованими в голові підшлункової залози. Середній вік становив 68 років (діапазон, 50-78 років). Клінічним проявом був біль у животі (100% пацієнтів), повторний панкреатит (60%), втрата ваги (30%), жовтяниця (30%). Комп’ютерна томографія (КТ) та магнітний холангіорезонанс (МРК) виявили TPMI-R у 8 пацієнтів (кістозна пухлина між 3-4 см у зв’язку з протокою Вірсунга) та комбінацію TPMI-CP та TPMI-R у 13 пацієнтів ( розширення протоки підшлункової залози> 5 мм у всіх випадках та разом з інтрамуральними вузликами розміром> 30 мм у 4 пацієнтів).
Цефалічну дуоденопанкреатектомію за методикою Уіппла виконували у групі з 13 пацієнтів через жовтяницю, виявляючи наявність атипії (5 пацієнтів) або інтрамуральних вузликів розміром> 30 мм (4 пацієнти) в ендоскопії FNA.
Консервативне хірургічне втручання в області дванадцятипалої кишки проведено у 8 пацієнтів з TPMI-R. У 4 пацієнтів виконана часткова резекція головки підшлункової залози із збереженням дванадцятипалої кишки згідно з методикою Pedrazzoli et al 8 (RPCP-PD), а у 4 пацієнтів - тотальна резекція головки підшлункової залози з сегментарною дуоденектомією (друга частина дванадцятипалої кишки) ), згідно з методикою Nakao 9 (RTCP-DS) (рис. 1 та 2).
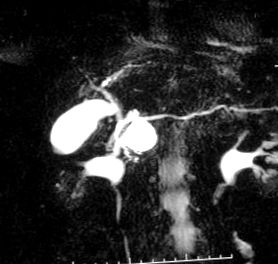
Рис. 1. Магнітний холангіорезонанс, що показує кістозну пухлину в голові підшлункової залози. Цей випадок лікували частковою резекцією головки підшлункової залози із збереженням дванадцятипалої кишки.
Рис. 2. Магнітний холангіорезонанс, що показує кістозну пухлину в голові підшлункової залози. Цей випадок лікували за допомогою тотальної резекції головки підшлункової залози за допомогою сегментарної дуоденектомії.
Методика RPCP-PD була розроблена в такі хірургічні часи:
1. Розсічення загальної печінкової артерії та розташування шлунково-дванадцятипалої артерії.
2. Збереження шлунково-дванадцятипалої артерії та її гілок, задньо-верхньої панкреатодуоденальної артерії та передньо-верхньої панкреатодуоденальної артерії.
3. Голова підшлункової залози мобілізується і звільняється від брижово-портальної осі.
4. Шийка підшлункової залози розділена, а головка підшлункової залози відведена вправо.
5. Розташований стовбур нижньої панкреатодуоденальної артерії. Внутрішньозадня панкреатодуоденальна артерія лігується, підтримуючи цілісність нижньої передньої панкреатодуоденальної артерії, яка забезпечує другу і третю частини дванадцятипалої кишки.
6. Загальна жовчна протока розташована біля її входу в головку підшлункової залози.
7. Головка підшлункової залози резекується від шийки до правої межі жовчної протоки, залишаючи відрізок тканини підшлункової залози (5-10 мм), що прилягає до дванадцятипалої кишки. Протока Вірсунга перев’язана в місці її з’єднання з жовчовивідною протокою (рис. 3). Сегмент підшлункової залози, що поступається сосочку Ватера, повністю резектований.
Рис. 3. Техніка часткової резекції головки підшлункової залози із збереженням дванадцятипалої кишки. Повне видалення сегмента підшлункової залози голови поступається сосочку Ватера.
8. Реконструкція шляхом анастомозу між тілом і хвостом підшлункової залози до товстої кишки (дукто-тонка кишка) у дефункціоналізованій петлі Ру-ен-Y (лівий 3-мм трансанастомотичний силастичний стент).
Методика RTCP-DS заснована на збереженні зрошення 4-5 см першого відділу дванадцятипалої кишки та третього відділу дванадцятипалої кишки з блоковою резекцією всієї головки підшлункової залози та другої частини дванадцятипалої кишки. Хірургічний час 1, 2, 3 і 4 при розробці методики ідентичний описаному в техніці RPCP-PD, за винятком того, що задньо-верхня та передньо-верхня панкреатодуоденальні артерії перев'язуються.
5. Наступним етапом є перев’язка та відділ загальної жовчної протоки, коли вона потрапляє в підшлункову залозу.
6. Розріз дистального кінця першого відділу дванадцятипалої кишки та відділ дванадцятипалої кишки на стику другого (нижче сосочка Ватера) і третього відділу дванадцятипалої кишки.
7. Лімфаденектомія ретропортальної території.
8. Жовчний міхур залишається in situ і зберігається 2 см загальної жовчної протоки.
9. У дефункціональній петлі Roux-en-Y реконструкція проводиться за допомогою панкреатично-порожнього кишкового анастомозу (дукто-тонка кишка), залишаючи трансанастомотичний 3-мм силастичний стент та кінцеву до бічної жовчі протоково-кишковий анастомоз (рис. 4-6).
Рис. 4. Техніка тотальної резекції головки підшлункової залози з сегментарною дуоденектомією. Шлунково-дванадцятипала артерія та її дванадцятипалої кишки, права гастроепіплоїдна артерія та її дванадцятипалої кишки збережені, а задньо-верхня та передньо-верхня панкреатично-дуоденальна гілки перев’язані, щоб зберегти васкуляризацію 4-5 см першої частини дванадцятипалої кишки. Збереження нижньої панкреатодуоденальної артерії та її гілки, нижньо-передньої панкреатодуоденальної артерії, що перев’язує нижньо-задню панкреатодуоденальну гілку, щоб зберегти третю частину дванадцятипалої кишки васкуляризованою.
Рис. 5. Блокова резекція головки підшлункової залози та другої частини дванадцятипалої кишки, включаючи великі та малі сосочки.
Рис. 6. Реконструкція з використанням дванадцятипалої кишки-дуоденостомії та дефункціональної петлі Roux-en-Y, панкреатоєюнального анастомозу з кінця в бік та холедохоеюнального анастомозу.
Проаналізовано інтраопераційні та післяопераційні фактори. Серед перших тривалість хірургічного втручання та крововтрата (необхідність переливання крові чи ні). Серед післяопераційних факторів загальні та місцеві ускладнення та середній термін перебування в лікарні. Нарешті, було проведено патологічне дослідження хірургічних зразків. Клінічне спостереження було різним. З 1995 по 2000 рік техніка Уіппла була технікою вибору. З 2000 року ми впровадили методику RPCP-PD та техніку RTCP-DS з листопада 2005 року по теперішній час.
У групі пацієнтів, які перенесли панкреатикодуоденектомію, середня тривалість операції становила 330 хв (діапазон - 240-360 хв). Жодному пацієнту не потрібно було переливання крові. Післяопераційні ускладнення виявились у 38%, в тому числі 1 ателектаз, 2 свищі підшлункової залози з низьким рівнем виходу (8, середня тривалість втручання становила 260 хв (діапазон, 200-290 хв). Жодному пацієнтові не було потрібно переливання крові Серед післяопераційних ускладнень один Пацієнт отримав фістулу підшлункової залози з низьким рівнем виходу (обговорення
Найважливішою складністю у виборі методу лікування ТПМІ є знання, чи є пухлина інвазивною чи ні. За допомогою рентгенологічних досліджень із використанням КТ або МРТ можна запідозрити злоякісні ураження, коли пухлина проникає в дванадцятипалу кишку або жовчну протоку, а також через наявність інтрамуральних вузлів або розширення протоки підшлункової залози .
CRM дуже корисний для розмежування між TPMI-CD та TPMI-R 13-18. В одній із серій з найбільшою кількістю пацієнтів з TPMI, Sohn et al 19 виявили, що неінвазивний TPMI був виявлений у 53% сортів TPMI-R, 22% у TPMI-CD та 25%, коли вони були присутні обидва патологічних різновиди. У цьому дослідженні інвазивний TPMI був виявлений лише у 25% TPMI-R, у 35% TPMI-CD та у 25%, коли були виявлені обидва ураження. Ці спостереження також були підтверджені в публікаціях Bernard et al 17 та Doi et al 20, які вказують на сорт TPMI-R як на той, що рідше представляє інфільтруючу аденокарциному порівняно з TPMI-CD.
Ендоскопічне ультразвукове дослідження у поєднанні з FNA дозволяє не тільки підтвердити дані рентгенологічних досліджень, але й встановити підозру на злоякісність шляхом вивчення клітинної архітектури пухлини. Ендоскопічна ретроградна холангіографія використовується японськими хірургами для дослідження злоякісних клітин у підшлунковому соку 13 .
Хірургічна резекція є вибором лікування для більшості пацієнтів з ІМТД. Виживання через 5 років після операції становить від 77 до 100% випадків, коли пухлина не є інвазивною 3. У 25% -45% випадків IMTD супутній інфільтруючій аденокарциномі. У цих випадках хірургічне втручання при раку, головна дуоденопанкреатектомія при пухлинах голови (Уіппл або з пілоричним щадінням), тілесно-дистальна панкреатектомія при пухлинах лівої підшлункової залози та повна панкреатектомія при дифузних ураженнях у поєднанні з регіонарною лімфаденектомією дозволяють досягти 5-річного виживання між 27% та 60% 3. Ця виживаність значно вища, ніж досягнута при хірургічному втручанні у пацієнтів із протоковою аденокарциномою підшлункової залози 21 .
Консервативне хірургічне втручання буде показано пацієнтам з TPMI-R, розташованим у голові підшлункової залози, та з патологічними ураженнями, такими як аденома, межа кордону та аденокарцинома in situ. Описана низка консервативних методик, які включають часткову резекцію головки підшлункової залози із збереженням дванадцятипалої кишки за методикою Бегера 7, часткову резекцію верхньої частини головки підшлункової залози із збереженням дванадцятипалої кишки разом із загальною резекцією нижньої частини підшлункової залози голова за методикою Педраццолі 8, ізольована резекція черевної підшлункової залози голови 22,23, тотальна резекція головки підшлункової залози з сегментарною дуоденектомією за методикою Nakao 9 та методикою Nakao, модифікованою Isaji et al 24. За винятком цієї останньої методики, усі вищезазначені часткові резекції головки підшлункової залози зі збереженням дванадцятипалої кишки мають основною проблемою те, що вони не забезпечують видалення TPMI через особливу дифузію пухлини до головного протоку та його гілок. У цих випадках ризик рецидиву пухлини може мати велике біологічне значення, якщо IMTD поєднувати з інфільтруючою аденокарциномою.
Частота фістули підшлункової залози була однаковою у 3 групах. У всіх випадках це були свищі з низьким виходом, контрольовані за допомогою консервативного лікування. Необхідно враховувати можливість цього ускладнення, тому доцільно залишити дренажні труби однією зверху та однією під панкреатично-тоничним анастомозом.
Анатомопатологічне дослідження вирізаних шматочків після використання консервативних методів резекції підшлунково-дванадцятипалої кишки показало відсутність інвазивної карциноми у всіх випадках. Середнє спостереження за цими пацієнтами було мінливим, 22 місяці (інтервал, 6-36 місяців) за допомогою методики RPCP-PD, яку ми впровадили у свою практику у 2000 році, та 4 місяці (інтервал, 2-6 місяців) за методикою CPRT -DS. У цьому короткостроковому спостереженні рецидивів пухлини не спостерігалося. У групі пацієнтів із втручанням Уіппла середнє спостереження становило 52 місяці (діапазон - 6-120 місяців). У цій групі лише один пацієнт з інвазивним TPMI помер через 5 років після операції з метастатичним захворюванням.
Цефалічна дуоденопанкреатектомія є методом вибору у випадках TPMI з підозрою на злоякісне ураження. Консервативне хірургічне втручання у пацієнтів з TPMI-R, розташованим переважно в голові підшлункової залози, обґрунтоване високою частотою доброякісних уражень. Тотальна резекція головки підшлункової залози з сегментарною дуоденектомією, у деяких випадках, має переваги перед частковими методами резекції головки підшлункової залози із збереженням дванадцятипалої кишки, що є більш анатомічним втручанням; головка підшлункової залози, де розташована пухлина, повністю резектована і має можливість проведення лімфаденектомії ретропортальної області. RTCP-DS мав нижчу післяопераційну захворюваність і коротший термін перебування в лікарні.
Кафедра хірургії. ICMD. Лікарняна клініка Барселони. Університет Барселони. Барселона. Іспанія.
Листування: професор Л. Фернандес-Крус.
Кафедра хірургії. Лікарняна клініка.
Університет Барселони.
Вільярроель, 170. Сходи 6, 4 поверх. 08036 Барселона. Іспанія.
Електронна адреса: [email protected]
Рукопис отриманий 27.04.2006 та прийнятий 07.04.2006.
- Лікування пухлини Клацкін
- Результати через 5 років; виведення os; n біліопанкре; Етика Ларрада у лікуванні ожиріння
- Лікування розсічення; n ізольований; симптом; етика; вісцеральні артерії; Доцільно
- Почервоніння піхви, профілактика, причини та лікування
- PRX-T33 - перша відновлююча процедура без голок