Іспанська асоціація педіатрії має одним з головних завдань розповсюдження суворої та сучасної наукової інформації з різних областей педіатрії. Anales de Pediatría є Науковим висловлювальним органом Асоціації і є засобом, за допомогою якого співробітники спілкуються. У ньому публікуються оригінальні роботи з клінічних досліджень у педіатрії з Іспанії та країн Латинської Америки, а також оглядові статті, підготовлені найкращими професіоналами кожної спеціальності, щорічні повідомлення про конгрес та щоденники Асоціації, а також посібники для дій, підготовлені різними товариствами/спеціалізованими Секції, інтегровані в Іспанську асоціацію педіатрії. Журнал, орієнтир для іспаномовної педіатрії, індексується у найважливіших міжнародних базах даних: Index Medicus/Medline, EMBASE/Excerpta Medica та Index Médico Español.
Індексується у:
Index Medicus/Medline IBECS, IME, SCOPUS, Індекс наукового цитування розширений, Звіт про цитування журналів, Embase/Excerpta, Medica
Слідкуй за нами на:
Фактор впливу вимірює середню кількість цитат, отриманих за рік за твори, опубліковані у виданні протягом попередніх двох років.
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
Вперше описаний у 1964 р. 1, синдром Швахмана-Даймонда (ССД) є рідкісним аутосомно-рецесивним захворюванням, приблизна частота випадків - 1 на 100 000 народжень 2,3, а співвідношення чоловіків і жінок - 1,7: 1 3, 4. Це друга причина вродженої екзокринної недостатності підшлункової залози в дитячому віці після муковісцидозу.
ССД - це мультисистемне захворювання, яке характеризується екзокринною недостатністю підшлункової залози, дисфункцією кісткового мозку, змінами скелета та низьким рівнем 2,5-8. Прогноз пацієнтів визначається повторюваними бактеріальними інфекціями, вторинними, головним чином, за рахунок зміни нейтрофілів, а також порушенням функції хребта та лейкемією.
Нещодавно ген SBDS був визначений як ген, відповідальний за SSD. Цей ген був розташований на рівні хромосоми 7, в локусі 7q11 5,9,10 .
У цій статті ми збираємось описати клінічний випадок немовляти, у якого в нашій службі був діагностований цей синдром.
14-місячне немовля направляється до нашої служби для дослідження гіпертрансаміназемії та застою ваги з 9-місячного віку.
Дитина не представила жодної відповідної сімейної чи особистої історії. Вага при народженні становила 3390 г, а зріст - 51 см. Він представив адекватний нормативний розвиток ваги до 9-місячного віку, після чого у нього почали з'являтися 4-5 липких, прогірклих стільців на день разом із встановленою законом стагнацією ваги.
Внаслідок цього стану його педіатр провів аналіз, в якому виділялися лише GOT 464 U/l та GPT 514 U/l. Він також мав деякі маркери целіакії, які були нормальними.
Через три місяці через стійкість гіпертрансаміназемії його направили до нашої служби для вивчення.
Фізичне обстеження виявило гармонійний мікросомальний вигляд з вагою та зростом нижче 3-го процентиля. Решта обстеження була нормальною.
Проведені додаткові випробування:
Гемограма: 8400 лейкоцитів (N, 16%; L, 77%; M, 5,8%), гематокрит 34,6%, гемоглобін 11,6 г/дл і 313 000 тромбоцитів.
Загальна біохімія: GOT, 417 од/л; GPT, 440 Од/л; нормальний білірубін, GGT та лужна фосфатаза.
Нормальний тест на піт.
Ван де Камер: відсутність стеатореї. Еластаза в калі 11,5 мкг/г.
Серологія вірусного гепатиту, 1-антитрипсин, нормальний метаболізм міді та цинку.
УЗД черевної порожнини: сильно виражена підвищена щільність підшлункової залози, що свідчить про екзокринну недостатність підшлункової залози.
Підводячи підсумок, ми знайшли картину екзокринної недостатності підшлункової залози, діагностованої практично не виявленою еластазою в калі та сумісним ультразвуковим дослідженням, із звичайним тестом поту, повтореним двічі. Крім того, у дитини спостерігалася затримка росту та легка нейтропенія. З підозрою на SSD ми продовжили проводити нормальне рентгенологічне дослідження кісток і генетичне дослідження, яке визначило, що дитина була гетерозиготом, що складається з двох мутацій гена SBDS (258 + 2T> C/183-184TA> КТ), за допомогою якого ми ставимо діагноз ССД у дитини.
Також було проведено генетичне дослідження у батьків, в результаті чого батько переніс мутацію 183-184 TA> CT, а мати - мутацію 258 + 2T> C.
З огляду на діагноз було розпочато лікування ферментами підшлункової залози та жиророзчинними вітамінами, покращуючи зовнішній вигляд стільця, але не розвиток ваги, підтримуючи вагу та зріст нижче 3-го процентиля.
Кількість нейтрофілів змінювалася, досягнувши цифри 540 нейтрофілів.
Клінічний фенотип ССД дуже неоднорідний, демонструючи широкий спектр клінічних проявів. Центральними ознаками синдрому є екзокринна недостатність підшлункової залози та дисфункція спинного мозку, обидва необхідні для постановки діагнозу 2,11. Аналогічним чином, затримка росту та зміни скелета характерні 2,11,12 .
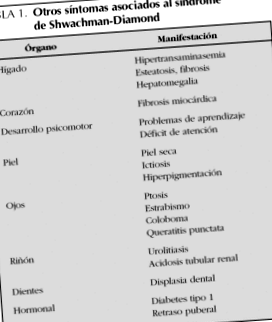
Інші можливі виявлення SSD наведені в таблиці 1. Зміни шкіри, очей та нирок дуже рідкісні.
Перші симптоми та ознаки ССД зазвичай з’являються на першому році життя, як це буває у нашого пацієнта 3 .
Коли діагноз ставлять у дитячому віці, дисфункція підшлункової залози присутня практично у всіх випадках. Низькі концентрації амілази (50-75% пацієнтів), низький вміст трипсиногену в сироватці крові (70-98%) та змінений тест на стимуляцію підшлункової залози (100%) є типовими 2,4. В даний час визначення фекальної еластази є найефективнішим тестом для оцінки недостатності підшлункової залози через її високу специфічність та чутливість та через те, що її значення не змінюються при прийомі ферментів підшлункової залози. Важкою недостатністю підшлункової залози вважається рівень еластази в калі нижче 100 мкг/г стільця 3. Що стосується візуалізаційних досліджень, то на УЗД черевної порожнини виявляється підшлункова залоза нормального або зменшеного розміру з підвищеною ехогенністю. КТ виявляє ліпоматоз підшлункової залози 14. У нашому випадку діагноз був поставлений з еластазою стільця 11,5 мкг/г разом із сугестивним УЗД.
Залучення підшлункової залози зазвичай покращується з віком у 40-60% випадків, мабуть, через збільшення секреції ліпази з віком 2,8 .
Найбільш частою гематологічною знахідкою є інтермітуюча нейтропенія, яка з’являється у 85-100% випадків 2,15,16. Незалежно від загальної кількості нейтрофілів, їх міграція також змінюється, тому існує підвищений ризик серйозних бактеріальних інфекцій навіть при нормальній кількості нейтрофілів 11,17. Поява інфекцій визначає прогноз у дитячому віці 18. Наша дитина представила цифри до 500 нейтрофілів за свою еволюцію, які спонтанно відновилися.
Інші гематологічні зміни, які можна виявити, - це анемія (50-80%), підвищена концентрація фетального гемоглобіну (80%) та тромбоцитопенія (25-85%) 15,19 .
Затримка росту спостерігається у 60% дітей і не залежить від порушення всмоктування з боку травлення, оскільки воно не покращується ні при підживленні ферментів підшлункової залози, ні при нормалізації функції підшлункової залози, яка може з’явитися з віком. Типовим є зріст і вага нижче 3 8,15 процентиля. Здається, затримка пов’язана з невід’ємною проблемою зростання 2. На даний момент наш випадок не показав поліпшення зросту, незважаючи на добавки ферментів підшлункової залози, і спостерігається в ендокринологічній консультації для відстеження розвитку висоти.
Кісткові зміни можуть виявлятися у 50-75% пацієнтів, хоча нещодавня стаття, що розглядає рентгенологічні зміни у 15 пацієнтів, виявляє зміни практично у всіх пацієнтів 12. Найбільш частими виявленнями є короткі ребра з костохондральним потовщенням, звуженням грудної клітки, більш очевидним у дітей у віці до 2 років, і метафізарна хондродисплазія довгих кісток (особливо в області стегон і колін) 11, більш очевидна у дітей старше 2 років 6 років. Інші висновки: затримка появи вторинних центрів окостеніння, генералізована остеопенія, аномальна трубочка довгих кісток, особливо великогомілкової кістки та першої п'ясткової кістки, клінодактилія, синдактилія та вальгусна деформація колін та стегон. У нашої дитини не відбулося жодних змін у проведеній кістковій серії, що може бути пов’язано з тим, що дитина була дуже маленькою на момент її проведення.
Інші можливі дані - підвищений рівень трансаміназ та гепатомегалії, які зазвичай спостерігаються в перші роки життя та, як правило, покращуються без ускладнень з віком. У нашому випадку гіпертрансамінамія була причиною звернення до нашої консультації.
Недавні дослідження показують, що мутації гена SDBS є у більшості пацієнтів із ССД 9,20. Цей ген був розташований у хромосомі 7, у локусі 7q11. Дві найбільш часто ідентифіковані мутації в медичній літературі гена SBDS (183-184 TA x CT [K62X] та IVS2 (258) + 2T x C [C84fs]) збігаються з тими, що були представлені нашою дитиною 5,21,22. Кожен з батьків був носієм однієї з двох описаних мутацій.
Щодо лікування, втручання проводитимуться за такими напрямками:
1. Добавка ферментів підшлункової залози та жиророзчинних вітамінів.
2. Профілактика та лікування інвазивних інфекційних захворювань з раннім лікуванням гарячкової хвороби.
3. Корекція гематологічних відхилень, коли це можливо.
4. Спостереження та лікування ортопедичних деформацій.
Важку нейтропенію або рецидивуючі інфекції можна лікувати за допомогою фактора, що стимулює колонії гранулоцитів (G-CSF) 16. Однак існують суперечки щодо можливості прискорення розвитку мієлопроліферативних синдромів 2,11 .
Переливання крові може знадобитися пацієнтам з анемією або симптоматичною тромбоцитопенією. Еритропоетин також може бути корисним для лікування анемії.
Гормон росту пробували без хороших довгострокових результатів 23 .
Трансплантація кісткового мозку є єдиним лікувальним варіантом при важкій дисфункції спинного мозку і рекомендується пацієнтам з важкою панцитопенією та лімфопроліферативним та мієлопроліферативним синдромами 11,24-26 .
Прогноз цього захворювання визначається інфекціями 27 та появою гематологічних новоутворень. Найбільш частими трансформаціями є гострий мієлоїдний, гострий лімфоїдний та ювенільний хронічний мієлоїдний лейкоз 2,3,7. За оцінками, цей ризик малігнізації становить близько 25% 3,4. Ризик вищий у дітей з прогресуючою панцитопенією. Середня виживаність цих пацієнтів оцінюється приблизно в 35 років 28 .
- Кропив'янка від fr; або і целіакія у дитячого пацієнта; trico Annals of Pediatrics
- S; синдром мікродуплікації; n 3q29 Аннали педіатрії
- Харчові рекомендації для дитини; або Аннали педіатрів спортсменів
- Пухлини нирок в ni; менше одного року; o Аннали педіатрії
- Лікування бактеріального менінгіту Аннали педіатрії