Вступ
Ожиріння - поширене захворювання, яким страждають понад 300 мільйонів дорослих людей у всьому світі [1]. Він визначається як індекс маси тіла (ІМТ), що перевищує 30. У Канаді поширеність ожиріння зросла майже в 3 рази за останні 2 десятиліття [2]. Приблизно 25% населення Канади класифікується як ожиріння [3].
Сучасні варіанти баріатричної хірургії класифікуються за кількома принципами. Суто обмежувальні процедури включають лапароскопічну регульовану пов’язку шлунка та шлункову шлунку. Шлункове шунтування Roux-en-Y - це обмежувальна операція з незначним підходом до мальабсорбції. Переважно мальабсорбційні процедури з обмежувальним компонентом включають перехід дванадцятипалої кишки та біліопанкреатичну диверсію. Майже суто мальабсорбційні процедури включають шлунково-кишковий шунтування.
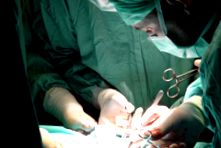
Лапароскопічна гастректомія рукавів (ГМЛ), також відома як поздовжня або вертикальна резекція шлунка, є відносно новим та ефективним хірургічним варіантом для лікування патологічного ожиріння (рис. 1). Спочатку він був запроваджений в 1990 р. Як альтернатива дистальній шлунково-кишковій трафіці за допомогою дуоденальної процедури з метою зменшення рівня ускладнень [4,5]. Вперше гастректомія рукава була виконана лапароскопічно Рен та співавт. У 1999 р. [6]. На той час ГМЛ вважався першою стадією у пацієнтів із високим ризиком до біліопанкреатичної диверсії або шлункового шунтування Roux-en-Y [7]. Згодом було визнано, що ГМЛ є ефективним як одна процедура для лікування патологічного ожиріння [8]. Хоча ГМЛ діє як обмежувальна процедура, він також може спричинити насичення на ранніх термінах, видаливши ділянку шлунку, що виробляє грелін [9].
РИСУНОК 1: Рукава гастректомія
Частота ожиріння в Канаді зростає, і все більше пацієнтів проходять баріатричні процедури [10]. Цей ріст ускладнюється зростаючою частотою медичного туризму, коли пацієнти виїжджають за кордон для хірургічної допомоги, зокрема баріатричної хірургії [11]. Це неминуче призводить до більшої частоти ускладнень, пов’язаних з такими процедурами. Тому дуже важливо, щоб усі хірурги, включаючи тих, хто практикує в менших громадах, усвідомлювали ці потенційні ускладнення та мали базове розуміння того, як ними керувати та коли шукати керівництва баріатричного хірурга. Мета цієї статті - пролити світло на основні принципи лікування ускладнень після ГМЛ. Автори представляють свій хірургічний підхід до ГМЛ та оглядають основні гострі (протягом 2 тижнів після операції) та пізні ускладнення, які можуть виникнути у пацієнтів після ГМЛ (табл. 1).
• ТАБЛИЦЯ 1: Ускладнення, пов'язані з лапароскопічною гастректомією рукавів (Див. Таблицю)
Хірургічна техніка
Пацієнта поміщають у лежаче положення, розставивши руки. Пневмоперитонеум виконують із закритою методикою, при цьому гострий Верес поставлений у ліву підреберну область живота. Два 10-мм порти розміщені в надпупковій та лівій середині живота. Додатковий порт розміром 15 мм розміщений у правій середині живота, щоб вставити степлер. Нарешті, 2 додаткові 5-міліметрові отвори розміщені у верхньому лівому та правому квадрантах живота. Ліву частку печінки медіально відокремлюють за допомогою ретрактора Натансона, розміщеного в області субксифоїда.
РИСУНОК 2: Рентгенограма, що показує нормальне зображення шлунка після лапроскопічної гастректомії рукава
Гострі ускладнення
Крововилив
Ризик післяопераційних кровотеч повідомлявся між 1% та 6% після ГМЛ [4,12]. Походження кровотечі може бути внутрішньосвітловим або позасвітловим. Внутрішньопросвітня кровотеча з основної лінії зазвичай проявляється кровотечею з верхніх відділів шлунково-кишкового тракту. Загальні симптоми включають гематемез або стілець мелени. Діагностика та лікування внутрішньосвітлової кровотечі дотримується загального алгоритму кровотечі з верхніх відділів шлунково-кишкового тракту. Це включає встановлення великопрофільних внутрішньовенних ліній для реанімації рідини, введення еритроцитів, якщо це необхідно, вимірювання виділення сечі з введенням катетера Фолі та термінову гастроскопію для діагностики та контролю джерела кровотечі.
Екстралюмінальна кровотеча зазвичай проявляється послідовним зниженням рівня гемоглобіну або ознаками тахікардії або гіпотонії. Загальне походження екстралюмінальної кровотечі включає шлункову основну лінію, селезінку, печінку або черевну стінку в місцях потрапляння троакарів. Автори пропонують лапароскопічний другий вигляд у всіх пацієнтів із позасвітковою кровотечею зі стійким серцебиттям більше 120 ударів на хвилину та післяопераційним падінням гемоглобіну більше 10 г/л. Термінова лапароскопія полегшує діагностику та дозволяє евакуювати згустки, а також проводити хірургічний контроль джерела кровотечі. Багато разів справжнє походження крововиливу неможливо встановити, але вони вважають, що евакуація гематоми та розміщення закритого всмоктувального стоку часто служать корисним доповненням до реанімації пацієнта.
Витік лінії зшивання
Витікання шлунка - одне з найсерйозніших ускладнень ГМЛ (рис. 3). Це трапляється у 5% пацієнтів після ГМЛ [8,12]. Існує декілька класифікацій, заснованих на рентгенологічних даних та на часі діагностики [15]. На основі контрастного дослідження верхніх відділів шлунково-кишкового тракту шлункову фільтрацію можна класифікувати на 2 типи. Тип I або субклінічний витік контролюється за допомогою хірургічного дренажу або через свищевий тракт у черевній або грудній порожнині. Тип II або клінічний витік - це поширений витік з дифузією контрасту в черевній або грудній порожнині [16]. Залежно від часу діагностики витоки шлунку класифікуються як ранні або пізні. Рання витікання зазвичай діагностується протягом перших 3 днів після операції, тоді як пізня витікання зазвичай діагностується більше ніж через 8 днів після операції [17].
• РИСУНОК № 3: рентген, що показує витік після ГМЛ
Витоки шлунка можуть бути діагностовані випадково або у звичайних серіях верхніх відділів шлунково-кишкового тракту, що проводяться післяопераційно без будь-яких клінічних ознак, або під час дослідницької лапароскопії/лапаротомії, що проводиться при незрозумілій тахікардії. У дослідженні Kolakowski et al. [18], було виявлено, що поєднання клінічних ознак лихоманки, тахікардії та тахіпное є 58,33% чутливими та 99,75% специфічними для виявлення витоків анастомозів. Цукровий діабет та апное сну були пов'язані з більшою частотою витоків анастомозів. Тому автори даної роботи пропонують діагностичну дослідницьку лапароскопію для пацієнтів, які виявляють ці 3 ознаки в ранньому післяопераційному періоді. За наявності витоку слід провести промивання черевної порожнини з хірургічним усуненням витоку (якщо це технічно можливо) та встановленням ентерального шляху годування. Оскільки шлунок обмежений у розмірах, переважним вибором для ентерального харчування є, як правило, їжуностомія годування.
Навпаки, лікування затримки витоку шлунку є складнішим хірургічним шляхом через наявність запальної реакції. За такого сценарію спроби відновити свищ, як правило, марні. Варіанти лікування включають консервативне або хірургічне лікування. Це залежить від гемодинамічного стану пацієнта та фізичних та рентгенологічних даних. За відсутності гемодинамічної нестабільності та фізичних даних, що свідчать про перитоніт, може бути розпочато консервативне лікування. Це включає реанімацію рідини, внутрішньовенне введення антибіотиків, відсутність прийому всередину, черезшкірне дренування внутрішньочеревних колекцій (якщо вони дренуються) та встановлення внутрішньосвіткового стента [19]. У септичного пацієнта з рентгенологічними ознаками витоку з дифузними зборами внутрішньочеревної рідини хірургічний дренаж гарантований.
У закладі, де працюють автори цієї роботи, пізні шлункові витоки успішно вправляються за допомогою дренажу (хірургічного або черезшкірного), встановлення шляху годівлі (ентерального або парентерального) та встановлення шлункових стентів протягом приблизно 2–4 тижнів (рис. . 4). Інші дослідники також застосовували внутрішньосвітлові стенти для управління витоками шлунку [20,21]. Гімппенс та ін. [20], повідомили про свій досвід ведення 29 пацієнтів із витоком шлунку після ГМЛ із стентуванням. Ці дослідники залишали стент на місці в середньому на 7 тижнів. Негайний успіх спостерігався у 19 пацієнтів після встановлення першого стента, тоді як 5 пацієнтам потрібно було встановити другий стент. Двоє пацієнтів мали постійні витоки і вимагали хірургічного втручання.
РИСУНОК № 4: Рентгенографія, що показує внутрішньосвітловий стент для лікування витоку після ГМЛ
Абсцес
Внутрішньочеревний абсцес - ще одне можливе ускладнення ГМЛ. Зазвичай він проявляється симптомами болю в животі, лихоманки/ознобу або нудоти та блювоти. Якщо є клінічні підозри, слід отримати КТ живота, щоб виключити наявність внутрішньочеревного абсцесу. У серії із 164 пацієнтів, які перенесли ГМЛ, Lalor та співавт. [22], повідомили про 1 пацієнта з абсцесом (0,7%). Лікування включає черезшкірне дренування та антибіотики.
Хронічні ускладнення
Стеноз
Формування стенозу - ще одне можливе ускладнення, яке виникає після ГМЛ. Це може статися як гостро після операції, через набряк тканин, або, частіше, пізно. Симптоми включають непереносимість їжі, дисфагію або нудоту та блювоту. Хоча повідомлялося про перекручення шлунка після ГМЛ [23], найпоширенішим місцем стенозу є incisura angularis [24]. Дослідження верхніх відділів шлунково-кишкового тракту або ендоскопія, як правило, є діагностичними.
Варіанти лікування залежать від часу пред’явлення. Гостро діагностована стриктура іноді піддається лікуванню консервативними методами: спокій кишечника (нічого через рот), регідратація внутрішньовенними рідинами та ретельне спостереження. За відсутності інших патологій (наприклад, абсцесу, витоку), ці стриктури спонтанно розсмоктуються без необхідності додаткового втручання. Невдача консервативного лікування гарантує ендоскопічну дилатацію.
Навпаки, хронічні стриктури, як правило, вимагають додаткового втручання. Це включає ендоскопічне або хірургічне лікування. Варіанти лікування залежать від тривалості стенозу. Ендоскопічна дилатація є безцінним інструментом, що застосовується у цій ситуації для стенозу короткого сегмента [25]. Послідовне лікування з інтервалом 4-6 тижнів є достатнім для лікування стенозу та поліпшення симптомів пацієнта. На відміну від цього, стеноз довгих сегментів та відмова ендоскопічного лікування вимагають хірургічного втручання. Варіанти включають лапароскопічну або відкриту сероміотомію або перехід на шлунковий шунтування Roux-en-Y. Дапрі та ін. [26], повідомили про свій досвід лапароскопічної сероміотомії у пацієнтів, які перенесли ГМЛ. Ці дослідники повідомили про успішні результати такого лікування. Парих та ін. [25], повідомили про 3,5% випадків симптоматичного стенозу після ГМЛ у їх серії із 230 пацієнтів; 2 пацієнти потребували переходу на шлунковий шунтування Roux-en-Y через неефективність ендоскопічного лікування.
Нестачі харчування
Дефіцити поживних речовин є загальними після баріатричної хірургії. Етіологія є багатофакторною через порушення всмоктування та зменшення прийому всередину. В недавньому дослідженні Gehrer et al. [27], поширеність дефіциту вітаміну В12, вітаміну D, фолієвої кислоти, заліза та цинку була зареєстрована у 3%, 23%, 3%, 3% та 14% відповідно після ГМЛ. Загалом, ці дослідники виявили, що дефіцит мікроелементів був менш поширеним після ГМЛ, ніж після шлункового шунтування Roux-en-Y; однак дефіцит фолатів був дещо частішим після ГМЛ, ніж при шунтуванні шлунка Roux-en-Y (22% проти 12%) [27]. Тому регулярне дослідження крові після ГМЛ для діагностики нестачі вітамінів та мінералів є обов’язковим. В установі авторів цього дослідження рівні пацієнтів у сироватці крові вітаміну В12, вітаміну D, фолієвої кислоти, заліза та кальцію регулярно контролюються через 3, 6 та 12 місяців після операції та, при необхідності, лікують їх належним чином.
Гастроезофагеальна рефлюксна хвороба
Шлунково-стравохідна рефлюксна хвороба (ГЕРХ) - це стан, який часто спостерігається у населення баріатричної хірургії. Хоча відомо, що деякі операції, такі як шлунковий шунтування Roux-en-Y, пов'язані зі зниженою частотою післяопераційного рефлюксу, це суперечливо при ГМЛ. В недавньому систематичному огляді Chiu et al. [28], автори визнали дані непереконливими щодо впливу ГМЛ на ГЕРХ. З включених досліджень 4 показали підвищену частоту ГЕРХ після операції, тоді як 7 продемонстрували зменшення частоти ГЕРХ. Сертер та ін. [29], провели ретроспективне дослідження у пацієнтів, які перенесли ГМЛ, і виявили, що 47% пацієнтів мали стійкі (> 30 днів) симптоми ГЕРХ. Найбільш часто повідомляються симптоми включають печію (46%) та регургітацію (2%). Лікування пацієнтів із стійкою ГЕРХ включає лікування інгібіторами протонної помпи. Ці пацієнти потребують ретельного клінічного спостереження. Якщо симптоми не зникають, незважаючи на використання інгібіторів, автори цієї роботи зазвичай проводять гастроскопію для діагностики.
Завершення
ГМЛ - нова ефективна процедура хірургічного лікування патологічного ожиріння. Тому кількість пацієнтів, які проходять цю процедуру, буде і надалі збільшуватися. Базові знання про загальні ускладнення та доступні варіанти лікування є важливими для всіх практикуючих загальних хірургів. У цій статті наведено основний посібник з управління ускладненнями після ГМЛ. Шляхом ранньої діагностики та лікування цих ускладнень можна зменшити захворюваність та смертність пацієнтів.
♦ Коментар та короткий зміст: Доктор Родольфо Д. Альтруді
- Підтверджена постійна втрата працездатності для хворого ожирінням
- Міська рада видає книгу для допомоги людям із патологічним ожирінням Noticias de Cabra en
- Уряд Шотландії хоче зменшити ожиріння серед дітей на 50% до 2030 року Пекелія
- Британський уряд використовує Сімпсонів для боротьби з ожирінням
- Як засоби масової інформації заохочують ожиріння у дітей та деякі тактики боротьби з ним