РОЗКЛАД АПАРТАМЕНТУ
КІНЕТИЧНИЙ ДОСЛІД ДЛЯ ЛАБОРАТОРІЙ ВИЩОГО РІВНЯ
Болівійський приватний університет
Вступ.
Штучний підсолоджувач α-L аспатил-L-фенілаланін-L-метиловий ефір був предметом великої кількості експериментів, включаючи кілька аналізів, синтез та дослідження у відповідь на солодкість. Це дослідження описує кінетичне дослідження аспартаму у водному розчині. Експеримент застосовується для фізико-хімічних або біофізичних хімічних лабораторій, він також може бути використаний як подальше дослідження для аналізів, про які вже згадувалося. Враховуючи велику кількість застосувань цього компонента в дієтичних напоях, йогуртах і морозиві, існує великий інтерес до процесу розкладання.
Аспартам повністю метаболізується організмом, його гідролізація виробляє аспарагінову кислоту, метанол та фенілаланін.
Він використовується як низькокалорійний підсолоджувач і не викликає порожнин. Він використовується для підсолоджування різних продуктів харчування та напоїв, а також як столовий "цукор". Максимальна добова доза - 40 мг/кг.
Це найважливіший із нових штучних підсолоджувачів. Виявлений у 1965 році, спочатку він був дозволений для використання в США як настільний підсолоджувач, хоча з 1983 року він був дозволений у цій країні як добавка до широкого асортименту продуктів. Хімічно це генетично модифікований продукт, його молекула складається з трьох елементів (двох амінокислот і одного спирту): фенілаланіну (50%), аспарагінової кислоти (40%) і метанолу (10%). Фенілаланін розпадається на речовину, яка називається дикетопіперазин (ДКП), що викликає пухлини мозку.
Опис експерименту.
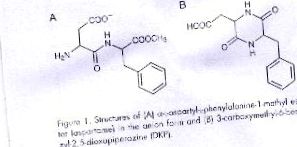
Аспартам у водному розчині розпадається на різноманітні продукти залежно від рН. При нейтральному або основному рН втрати метанолу переважають з утворенням 3-карбоксиметил-6-бензил-2,5-діоксопіперазину, зазвичай укороченого до 2,5-дикетопіперазину або ДКП і деякої кількості α-L-аспатил-L-фенілаланіну. У досліджуваному експерименті рН підтримується на рівні 7,0, де основним продуктом є DKP, а аспартам існує приблизно в 50:50 сумішах цвітеріону та аніонних форм. Наявність кінцевої аміногрупи у депротонованій формі необхідна для нуклеофільної атаки на карбоксильний вуглець, як показано на схемі I. Окрім залежності від рН, на діапазон також впливає ідентичність та концентрація буферної системи. Зокрема, спостерігається більший ступінь поліпшення, коли присутній фосфат, можливо, завдяки здатності віддавати і приймати протон одночасно, як показано на схемі I. У цьому експерименті буферний ефект досліджується шляхом вимірювання діапазону фосфату 0,20 М і 0,20 М цитрату, обидва з яких можна знайти в дієтичних напоях, але при значно нижчих концентраціях у комерційних продуктах. Фосфат також містить хлорид натрію для підвищення загальної іонної сили до 1,0 М.
Через постійні інтервали часу аликвоти по 100 мкл відбирають і переносять у пробірки, що містять 200 мкл розчину фосфатного буфера при 0,025 М і рН 3,0. Сукупні ефекти розведення, охолодження та зниження концентрації та рН буферного розчину зупиняють реакцію. Як можна швидше розведені аликвоти розділяють на колонці зі зворотною фазою С18 (хімічно пов'язана зворотна фаза, що складається з лінійних вуглеводневих ланцюгів з 18 атомами вуглецю)
і, як рухома фаза, суміш, що складається з 45% метанолу та 55% фосфатного буфера (водний) 0,025М з рН = 3. Перші аргументи отримуються шляхом побудови графіку ln (At-A∞) щодо часу, де At-A∞ - області піків аспартаму в моменти часу t та нескінченності відповідно.
Метанол у буферному розчині ВЕРХ може спричинити проблеми із зором та можливу сліпоту при вдиханні або попаданні всередину. При контакті зі шкірою може виникнути незначне подразнення або сухість.
Дикетопіперазин (ДКП) викликає пухлини головного мозку; Ось чому Управління з контролю за продуктами та ліками (FDA) наказало, щоб усі продукти, що містять аспартам, мали легенду "Фенілкетонурік: Містить фенілаланін". Аспарагінова кислота - ще один канцероген у цій суміші.
Третім компонентом є метанол, або деревний спирт. Цей алкоголь засліплює - або вбиває - тих, хто вживає алкогольні напої, підроблені або нелегально вироблені.
Потрапляючи в організм, метанол, який вже розкладається на формальдегід, щоб спробувати його усунути, зберігається в жировій тканині, а решта перетворюється на мурашину кислоту, інший канцероген. Це означає, що з кожним ковтком, що дається «легкій» або «дієтичній» соді, або будь-якому іншому продукту, що містить аспартам (жувальна гумка, йогурт, крупи, їжа, солодощі та навіть «ліки»), ви споживаєте три канцерогени: мурашина кислота, формальдегід та фенілаланін DKP, серед багатьох інших продуктів, що є результатом розпаду аспартаму в організмі.
Аргументи першого порядку для системи трьох отриманих реакцій показані на малюнку 2. Таблиця 1 містить діапазони постійних (Кобс) та енергій активації (Еа). Середня енергія активації становить 71,9 ± 8,5 кДж/моль, що вигідно порівнюється з результатом 58 ± 9 кДж/моль, отриманим Цубелі та Лабуфою з використанням 0,10 М фосфату та рН 7. Белл та Ветцель отримали константу діапазону 0,00352 + 0,00005 1/хв з використанням 0,20 М фосфату рН 7,0 при 25 ° C. Для цього експерименту для обчислення значення при 25 ° C використовували спостережену енергію активації та константу діапазону при 40 ° C. За даними таблиці 1 результат дорівнює 0,00461 + - 0,00061 1/хв, що є достатньо сумісним результатом з Беллом та Ветцелем.
Висновки
5.1. Висновки лабораторії.
Розкладання аспартаму - популярний експеримент для студентів фізико-хімічної та біофізичної хімії, який дає хороші результати. За умови ефективного використання часу проста група студентів може виконати експеримент у 5-годинній лабораторії. Припускаючи, що курс працює на обертовій системі. Для однієї групи студентів, які проводять експеримент щотижня, єдиним необхідним інструментарієм є рідинний хроматограф з ультрафіолетовим детектором із змінною довжиною хвилі, студенти можуть вивчити поняття хімічної кінетики та взаємозв'язок із споживанням продуктів, що зберігаються.
Особисті висновки.
Провівши дослідження та дізнавшись про реакцію аспартаму при розкладанні, важливо зазначити, що він не настільки шкідливий, як вважають, оскільки в комерційних продуктах він виявляється у концентраціях, значно нижчих, ніж ті, що розглядаються в лабораторії, але в в будь-якому випадку, це все ще смертельний ворог для людини, якого потрібно контролювати.
Також завдяки цьому дослідженню ми дізналися про хроматографи та їх роботу при аналізі речовин, в даному випадку аспартаму.
І нарешті, важливо знати середній час життя сполук, щоб вжити належних запобіжних заходів при споживанні певних хімічних сполук.
Бібліографія.
Журнал хімічної освіти - вип. 82 - No 6 червня 2005 р
"Солодка обіцянка або гірка реальність" - El Nuevo Diario - неділя, 13 листопада.
"Рідка хроматографія високого тиску". Х. М. Макнейр та Б. Есквівель. Наукова монографія ОАГ.
Важливі дані.
Синоніми: Метиловий ефір аспартил-фенілаланіну
Хімічна назва: α-L аспатил-L-фенілаланін-L метиловий ефір
E-номер: E 951
Хімічна формула: C14H18N2O5
Відносна молекулярна маса: 294,31
Опис: Білий кристалічний порошок без запаху із солодким смаком, приблизно в 200 разів солодший за сахарозу.
Розчинність: Легко розчинний у воді та етанолі.
Втрати при висиханні: Не більше 4,5% (105 ° С, 4 години).
Сульфатна зола: не більше 0,2% сухої маси.
рН: від 4,5 до 6,0 (розчин 1 на 125).
Миш'як: не більше 3 мг/кг у сухому вазі.
Свинець: не більше 1 мг/кг у сухому вазі.
Важкі метали: Не більше 10 мг/кг, виражене в Pb в сухому вазі.
5-бензил-3,6-діоксо-2-піперазин-цетинова кислота: не більше 1,5% сухої маси.
- Тут ви знайдете інформацію про картку Insuficiencia; тут для вашої школи Заходьте зараз! Vago Corner
- Введіть сюди, якщо ви шукаєте БЕЗ ГЛЮТЕНОВОЇ БОРОШИНИ, придатної для целіакії
- Інформація для сімей CEIP SAN WALABONSO 2019
- Це продукти, які слід їсти для боротьби з в’ялістю - інформація
- Факти живлення насіння льону та користь для здоров’я