Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
Аргентинське товариство радіології (SAR) буде опубліковане видавством Thieme з січня 2018 року. Інтернет-платформа для подання рукописів розробляється і повинна бути доступна в 3-му тижні січня. З цього моменту нові рукописи та редакції будуть оброблятися в новому редакторі редакцій (http://www.editorialmanager.com/rar/default.aspx). Аргентинський журнал радіології щиро вибачається за незручності.
Тим часом, якщо у вас виникли запитання, будь ласка, зв'яжіться з Габріелем Мартінсом ([email protected]). Незабаром з’являться нові оновлення.
Revista Argentina de Radiología (RAR) буде видаватися видавцями Thieme з січня 2018 року. Платформа онлайн-подання переробляється та передається, і, як очікується, вона почне працювати 3-го тижня січня 2018 р. Звичайна подача рукописів та звітів рецензентів буде оброблятися з цього моменту в новій редакційній системі (на http: // www .editorialmanager.com/rar/default.aspx). Журнал Revista Argentina de Radiología (RAR) щиро вибачається за короткий період незручностей.
Тим часом, якщо у вас виникли запитання, будь ласка, зв'яжіться з Габріелем Мартінсом ([email protected]). Більше оновлень, які слідкувати найближчим часом.
Індексується у:
Index Medicus Latinoamericano (LILACS), Latindex, Núcleo Básico de Magazines del CONICET, SciELO та Scopus.
Слідкуй за нами на:
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Огляд теми
- Патологічна анатомія
- Візуалізація
- Диференціальна діагностика
- Лікування та спостереження
- Етичні обов'язки
- Захист людей і тварин
- Конфіденційність даних
- Право на приватність та інформовану згоду
- Конфлікт інтересів
- Бібліографія
Аутоімунний панкреатит (ПАІ) - це окрема форма хронічного панкреатиту, що характеризується аутоімунним патогенним механізмом. Частота цього явища дещо вища у пацієнтів чоловічої статі (60%), а середній вік вилучення становить від 40 до 60 років, хоча віковий діапазон значно ширший (від 14 до 80 років). Гістологічно ПАІ має щільний запальний інфільтрат різної міри, який може бути вогнищевим або дифузно вражати всю підшлункову залозу. Його клінічна картина в більшості випадків є неспецифічною: слабкий біль у животі і рідко симптоми гострого панкреатиту, втрата ваги або жовтяниця. У кількох дослідженнях було описано залучення багатоорганів до аутоімунного процесу, що вказує на системну природу захворювання.
У 2011 році Міжнародний консенсус з діагностичних критеріїв аутоімунного панкреатиту (ICDC) встановив діагностичні вказівки або рекомендації, які передбачають, що магнітно-резонансна томографія (МРТ) та МР холангіопанкреатографія (MRCP) є основними методами діагностики.
У цій роботі ми представляємо візуалізаційні характеристики IAP, його диференціальний діагноз та результати візуалізації після лікування та спостереження. Окрім того, ми повідомляємо про наш досвід цієї неприємної та рідкісної хвороби.
Аутоімунний панкреатит (АІП) - це окрема форма хронічного панкреатиту, спричинена аутоімунним патогенетичним механізмом. Це вражає чоловіків (60%) дещо частіше і зазвичай трапляється між 40-60 роками, хоча можливий діапазон значно ширший (14-80 років). Гістологічно AIP характеризується наявністю щільного запального інфільтрату зі змінним розширенням. Він може бути вогнищевим або дифузним по всій підшлунковій залозі. Клінічні прояви в більшості випадків є неспецифічними: пацієнти мають легкий біль у животі, рідко симптоми гострого панкреатиту, втрату ваги та жовтяницю. У кількох дослідженнях повідомлялося про багаторазове ураження органів внаслідок аутоімунного процесу, вказуючи на системний характер захворювання.
У 2011 р. Міжнародні консенсусні діагностичні критерії для аутоімунного панкреатиту (ICDC) визначили керівні принципи, а магнітно-резонансна томографія (МРТ) та МР-холангіопанкреатографія (MRCP) стали еталонним діагностичним методом у діагностиці захворювання.
У цій роботі буде розглянуто характеристики візуалізації, диференціальний діагноз та особливості візуалізації після лікування та подальші дії. Крім того, переглядається наш досвід цієї незвичної та складної хвороби
Аутоімунний панкреатит (ПАІ) - це окрема форма хронічного панкреатиту, що характеризується аутоімунним патогенним механізмом. Sarles та ін. 1 були першими, хто описав цю сутність в 1961 році як хронічне запалення підшлункової залози можливої аутоімунної природи. У 1995 р. Йошида та співавт. 2 вперше ввів свою сучасну назву та описав основні характеристики: підвищений рівень імуноглобулінів у сироватці крові, інфільтрація лейкоцитів у тканину підшлункової залози, дифузний та нерегулярний стеноз головного протоку підшлункової залози, збільшення паренхіми підшлункової залози та наявність інших аутоімунних захворювань .
Хоча в наступні роки діагностичні труднощі призвели до встановлення різних діагностичних критеріїв, необхідно було універсально визначити клінічні, рентгенологічні та лабораторні дані 3–5. У 2011 році Міжнародний консенсус з діагностичних критеріїв аутоімунного панкреатиту (ICDC) узгодив керівні принципи, передбачаючи, що магнітно-резонансна томографія (МРТ) та магнітно-резонансна холангіопанкреатографія (MRCP) є основними методами діагностики. .
У цій статті ми повідомляємо про наш досвід щодо цієї проблематичної та рідкісної хвороби, оскільки наш заклад є довідковим центром для захворювань підшлункової залози, а наші рентгенологи мають знані знання щодо оцінки змін проток підшлункової залози та паренхіми 3,7–13 .
Огляд теми
ПАІ вважається рідкісним захворюванням підшлункової залози, що відповідає 7% випадків хронічного панкреатиту. З 2002 по 2015 рік у нашому закладі ми надали допомогу 186 пацієнтам, які постраждали від цієї організації.
З гістологічної точки зору ПАІ характеризується наявністю щільного запального інфільтрату зі змінним розширенням, який може бути вогнищевим або дифузно вражати всю підшлункову залозу з прогресуючим заміщенням паренхіми підшлункової залози внаслідок фіброзу. З цієї причини з морфологічної точки зору також виділяють вогнищеву і дифузну форму аутоімунного панкреатиту, хоча досі дискутується, чи є обидва типи двох різних стадій одного захворювання 3. .
Фокальна змінна представляється як експансивне ураження голови або тіла та хвоста підшлункової залози, і її диференціальна діагностика з новоутвореннями, головним чином аденокарциномою підшлункової залози, представляє проблему 15 .
Частота ВАД трохи вища у чоловіків (60%), а середній вік коливається від 40 до 60 років, хоча діапазон може бути набагато ширшим (від 14 до 80 років). У пацієнтів не було алкоголізму, жовчнокам’яної хвороби або запалення стінок дванадцятипалої кишки. Після нетривалого періоду терапії стероїдами настає швидка і значна ремісія симптомів та зникнення рентгенологічних та лабораторних досліджень 9,10,16 .
Симптоми в більшості випадків абсолютно неспецифічні: слабкий біль у животі і рідко симптоми гострого панкреатиту, втрати ваги або жовтяниці. У запущених формах можуть бути ознаки екзокринної недостатності підшлункової залози та діабету 17. Крім того, у кількох дослідженнях було описано залучення багатоорганів до аутоімунного процесу (що вказує на системну природу захворювання). Найчастіше уражаються органи - внутрішньо- і позапечінкова жовчна протока (68-88%), нирки (35%), слинні залози (12-16%) та заочеревина (3-8%). Також часто зустрічаються аутоімунні синдроми, такі як виразковий коліт, тиреоїдит Хашимото, склерозуючий холангіт, вузликова еритема та синдром Мікуліча.
Найбільш поширеними лабораторними даними є підвищений рівень аутоантитіл та імуноглобулінів G у сироватці крові, особливо типу 4 (IgG4), які зазвичай подвоюють норму. З цієї причини кілька авторів вважають, що ПАІ - це системне захворювання, пов'язане з IgG4 з переважним ураженням підшлункової залози. У зв'язку з цим IgG4 вважається корисним маркером для підтвердження діагнозу, проведення терапевтичного спостереження, виявлення пацієнтів з дуже важкою формою захворювання та оцінки ризику рецидиву 18,19. Інші лабораторні дані - це підвищення рівня ферментів підшлункової залози та печінки.
З рентгенологічної точки зору, навіть коли УЗД та комп’ютерна томографія (КТ) є хорошими діагностичними інструментами, в даний час МРТ вважається обраним методом візуалізації. Зміни сигналу підшлункової залози у зважених послідовностях Т1 та Т2 та динамічна оцінка після введення контрасту дозволяють ранню діагностику та правильну оцінку відповіді на лікування. Крім того, MRCP забезпечує оптимальне анатомічне зображення підшлункової та жовчовивідних систем протоки, сприяючи диференціальному діагнозу між ПАІ та новоутвореннями підшлункової залози 6 .
Найбільш типовим і значущим гістологічним аспектом ПАІ є наявність щільного інфільтрату, розташованого навколо міждолькових проток залозистих ацинулів. Це складається в основному з лімфоцитів і плазматичних клітин, а також макрофагів і тучних клітин. Утруднені протоки засмічуються, і їх епітелій, як правило, схожий на зірку або щілину. Взагалі, протокові стінки також потовщені фіброзом, який вистилає протоку і стає розвиненим міждольковим або внутрішньодольковим. В останньому випадку це спричиняє атрофію ацинарних клітин та ізоляцію острівців підшлункової залози 14,20 .
Замбоні та ін. 13 показали, що близько 50% пацієнтів з ПАІ реєструють додаткову гістологічну модифікацію: міофібробласти, які викликають запалення та набряки, із типовим псевдопухлинним виглядом 13,14,20,21. Крім того, можуть спостерігатися явища васкуліту і, рідше, артеріїту.
Відповідно до консенсусу Гонолулуської конференції, останньої гістологічної класифікації, ПАІ можна розділити на дві групи відповідно до її патології 21:
-
до)
ПАІ 1 типу: склерозуючий лімфоплазматичний панкреатит (PELP) або панкреатит без ураження гранулоцитарного епітелію (СЧВ). Відмінні гістопатологічні ознаки включають щільний перидуктальний лімфоплазматичний та плазмоклітинний інфільтрат, типовий сториформний фіброз, васкуліт з лімфоплазматичним інфільтратом та високу щільність IgG4-позитивних клітин плазми. Клінічно ця форма є проявом підшлункової залози системного синдрому, пов'язаного з IgG4, з високим рівнем IgG4 у сироватці крові та ураженням позашлункової залози, таким як склерозуючий холангіт, синдром Шегрена та ретроперитонеальний фіброз. В основному страждають пацієнти літнього віку (середній вік: 64), зазвичай чоловіки.
PAI типу 2: ідіопатичний центральний протоковий панкреатит (PDCI) або панкреатит із ВКВ. Він представляє перидуктальний лімфоплазмоцитарний інфільтрат, але без наявності васкуліту та сториформного фіброзу. Поширені гранулоцитарні ураження епітелію: тобто фрагменти епітелію міждолькових проток через інфільтрацію нейтрофілами, які можуть утворювати протокові абсцеси.
Хоча PELP асоціюється з підвищенням неспецифічного рівня аутоантитіл та рівня IgG4 у сироватці крові, PDCI не має остаточних аутоімунних серологічних маркерів і не пов'язаний з екстрапанкреатичними аутоімунними проявами. Так само, порівняно з PELP, PDCI вражає пацієнтів на десять років молодшими, без переважання статі.
Ця класифікація на дві гістопатологічні схеми широко застосовується японськими та північноамериканськими авторами 4,5,22 .
Візуалізація
Типовою знахідкою ПАІ є збільшення ураженої підшлункової залози. Завдяки щільному запальному інфільтрату уражена паренхіма збільшує свої розміри, втрачає фізіологічну долькову структуру і поступово заміщується масами-областями фіброзу 6,13,14,20,21. При дифузії PAI вражає всю підшлункову залозу з «ковбасоподібним» збільшенням і чітко визначеними межами; Хоча, якщо він є вогнищевим, крім того, що він менш поширений, він відрізняється наявністю вогнищевої маси в голові або в тілі та хвості підшлункової залози, яку важко діагностувати через подібність до аденокарциноми підшлункової залози 3,9, 10,12, 16 (рис. 1 і 2).
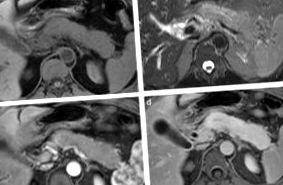
(а) У T1-зваженому градієнтному ехо-послідовності з придушенням жиру в осьовій площині спостерігається дифузне збільшення всієї підшлункової залози, яке виявляється гіпоінтенсивним порівняно з печінкою. (b) У зваженій за Т2 послідовності, з швидким одноразовим і напівфур’є-спіновим відлунням (HASTE) у осьовій площині, із придушенням жиру, уражена паренхіма виглядає гіперінтенсивно порівняно з паренхімою печінки. Після ін'єкції контрасту ураження виявляється (c) гіповаскулярним під час артеріальної фази, (d) із затримкою контрасту під час пізньої фази.
- Я переглянув; російська система; тика і s; наративний синтез втручань при ожирінні без ускладнень;
- Спалюйте жир завдяки 15-хвилинному кардіо-тренуванню для тіла та душі La Revista El Universo
- Ви можете спалити 1000 калорій за 1 годину, чи можете ви La Revista IN
- Небажані розлуки Журнал
- Сергій Корсаков - журнал «Галенус»