предметів
реферат
Білкові мутації альфа-синуклеїну (SNCA) пов'язані з хворобою Паркінсона. Нещодавно ми повідомляли, що немутовані SNCA збільшують засвоєння глюкози через шлях кінази Gab1-PI3-Akt та з'ясовують його вплив на регуляцію глюкози. Тут ми досліджували зв'язок SNCA з резистентністю до інсуліну (ІР), стан, що характеризується зниженим поглинанням глюкози в тканинах. Наші спостереження включають спостереження за популяційним дослідженням, а також модель миші з дефіцитом SNCA, яка раніше не характеризувалась у сценарії ІЧ. У 1152 пацієнтів ми виявили, що рівні SNCA у сироватці крові опосередковано корелювали з показниками ІЧ - індексом маси тіла, оцінкою гомеостатичної моделі ІР (HOMA-IR) та імунореактивного інсуліну (ІРІ) - і меншою мірою з артеріальним тиском та віком. ці миші з дефіцитом SNCA продемонстрували зміни у відповідях на глюкозу та інсулін під час ІР, викликаних дієтою. Крім того, під час оцінки еуглікемічних затискачів, нокаутовані миші SNCA, які харчувались дієтою з високим вмістом жиру (HFD), показали сильний ІР у жировій тканині та скелетних м’язах. Ці результати дають нові уявлення про ІР та діабет і вказують на SNCA як на потенційного кандидата для подальших досліджень.
Метаболічний синдром є одним із найпоширеніших результатів у клініці і вражає мільйони пацієнтів у всьому світі, що призводить до значного навантаження на системи охорони здоров’я у всьому світі 1, 2, 3. Цей синдром характеризується наявністю декількох факторів ризику та станів, які можуть спричинити порушення обміну речовин, включаючи гіпертонію, цукровий діабет 2 типу, ожиріння та дисліпідемію 4. Одним із таких станів є інсулінорезистентність (ІР), яка може призвести до цукрового діабету 2 типу. .
Детальний механізм ІР ще не з’ясований. Сприяючі гіпотези включають цитотоксичну дію пальмітату в периферичних тканинах 5, залежну від рецептора Toll-4 активацію NF-κB, глікемічну шкоду 7 та дисфункцію мітохондрій 8. Однак перший передбачуваний сприяючий фактор (пальмітат) привертає найбільшу увагу дослідників, що призводить до нових методів лікування, таких як рецептори G-білків (GPCR), орієнтованих на терапії (тобто агоністи GPR-40) 9 .
Альфа-синуклеїн (SNCA) - це білок, багатий нейронами та кровотворними тканинами і присутній у сироватці крові 10, 11, 12, 13, 14, 15. SNCA, як видається, функціонує в деяких з вищезазначених механізмів, що лежать в основі ІЧ. SNCA взаємодіє з ліпідами, такими як пальмітат, як транспортер 16 вільних кислотозв'язувальних білків (FABP), запобігає експресії гліоксалази I та пошкодженню глікації в нейрональних клітинах 17 і має безліч позамозкових функцій. SNCA нещодавно асоціюється з регуляцією глюкози, а також негативною секрецією інсуліну через модуляцію K-каналів у бета-клітинах підшлункової залози 18. Останнє вказує на те, що SNCA може відігравати роль у зменшенні гіперінсулінемії, яка спостерігається в таких станах, як ІЧ. Ми також раніше описували функцію SNCA у метаболізмі глюкози in vitro та in vivo за допомогою гетеродимерного рецептора ліпофосфатидної кислоти, пов'язаного з G-білком (LPAR2) - CD90 19; однак, як SNCA впливає на інсулін, не ясно. Це питання було предметом нашого розслідування.
Цікаво, що ми спостерігали раніше не повідомлений профіль SNCA, пов’язаний з ІР, як у людей, так і у гризунів.
результат
SNCA та IR у сироватці крові у людини
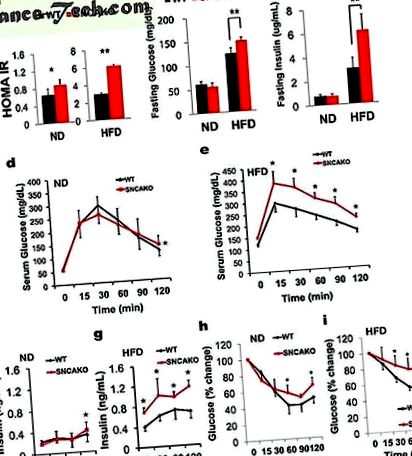
Миші SNCAKO демонструють порушення метаболізму глюкози під час дієти, індукованої ІЧ-дієтою
(а) Індекс оцінки гомеостатичної моделі резистентності до інсуліну (HOMA IR) у мишей WT та SNCAKO після 5 тижнів HFD. n = 10, кожна група. * P
У людей рівні SNCA в сироватці крові та HOMA-IR або IRI були суттєво і сильно корельовані. Низький рівень SNCA у сироватці крові чітко продемонстрував більш високий рівень HOMA-IR та інсуліну в сироватці крові, що відповідає профілю метаболізму глюкози у мишей, що нокаутують SNCA. Цікаво, що вони також корелювали DBP, ІМТ та вік (незначна кореляція); це може свідчити про те, що SNCA взаємодіє з іншими факторами ризику метаболічних захворювань поряд із HOMA-IR та IRI у людей. Ці взаємодії SNCA з іншими умовами, крім HOMA-IR та IRI, вимагають подальших досліджень і будуть предметом майбутніх досліджень нашої дослідницької групи.
Обмеження нашого дослідження популяції включають його дизайн поперечного перерізу. Перспективний підхід дозволить нам краще зрозуміти зв’язок між причинно-наслідковим зв’язком та SNCA у сироватці крові з часом, а також граничні значення для нормальних рівнів SNCA у сироватці крові. Крім того, оскільки це дослідження включало лише пацієнтів японського походження, наші висновки не можна узагальнити до інших етнічних груп. Потрібне подальше дослідження у пацієнтів з метаболічними захворюваннями або діабетом 2 типу, щоб оцінити можливий зв'язок між SNCA в сироватці крові та тяжкістю захворювання або ускладненнями.
Сильні сторони нашого дослідження включають велику популяцію, широкий діапазон клінічних характеристик пацієнтів, медичних працівників з великим досвідом попередніх паралельних клінічних досліджень у проекті Танно та Субецу, комплексну розробку (підходи людини та in vivo) та надійний статистичний аналіз .,
В даний час вузький терапевтичний миш’як проти ІР є основною проблемою для лікарів у зменшенні ризику розвитку ІР та/або діабету 2 типу, при якому реакція тканинного інсуліну сильно обмежена. Таким чином, SNCA може забезпечити нові шляхи до нових терапевтичних засобів при ІР та цукровому діабеті.
Матеріали і методи
матеріалів
Ми використовували рекомбінантний SNCA (Atgen, Південна Корея) та інсулін (Humulin-R100, Lilly, Японія). Анти-BSA (альбумін) був придбаний у компанії Upstate Biotechnology (США); всі інші антитіла були придбані у Cell Signaling (США).
Людське дослідження
Процедури для тварин
Експерименти були схвалені Комітетом з етики для експериментів на тваринах Медичного університету при Вищій медичній школі університету в Осаці. Всі експерименти in vivo проводились відповідно до норм для тваринницьких установ в Університеті Осаки. Ми використовували мишей однакової маси тіла для групових порівнянь. Інсулін у сироватці крові (Morinaga, Японія), глюкагон (R&D, США) та кортизол (Cayman Chemical Company, США) кількісно визначали методом ІФА.
методи
імуноблотинг
Зразки обробляли SDS-PAGE і переносили на мембрани PVDF. Потім мембрани блокувались у 5% знежиреному молоці та інкубували з відповідними антитілами. Ми оцінили хемілюмінесценцію, використовуючи Image Quant LAS4000 mini (GE, США).
Внутрішньочеревинний тест на толерантність до глюкози та інсуліну (ipGTT та ipITT)
Після 5 тижнів впливу HFD 32 та через 8 годин голодування мишам вводили глюкозу (2 г/кг) або інсулін (0,8 МО/кг). Зразки крові відбирали через 0, 15, 30, 60, 90 і 120 хвилин.
Глюкозний затискач
Після катетеризації серця та звикання мишей миші голодували протягом 5 - 6 годин. Потім, в еуглікемічних умовах, мишей WT та SNCAKO оцінювали за допомогою радіоактивно мічених показників. Забір крові та тканин проводили, як описано вище (див. Додаткові матеріали) 33, 34 .
Статистичний аналіз
Дані про людей аналізували за допомогою IBM SPSS Statistics 19. Ми використовували Stat View v5.0 як для даних in vivo, так і in vitro. Ми представили дані як середнє значення ± sd. Для статистичної значущості ми використовували тест t Стьюдента та ANOVA.
Детальніше
Як цитувати цю статтю: Родрігес-Араухо, Г. та ін. Низький рівень альфа-синуклеїну в крові пов'язаний з резистентністю до інсуліну. Наук. Респ. 5, 12081; doi: 10.1038/srep12081 (2015).
Додаткова інформація
Файли PDF
Додаткова інформація
Коментарі
Надсилаючи коментар, ви погоджуєтесь дотримуватися наших Загальних положень та умов та Правил спільноти. Якщо ви вважаєте, що це образливий вчинок, який не відповідає нашим умовам чи інструкціям, повідомте про це як про недоречний.
- Рекомендації - неінвазивне скринінгове дослідження крові матері
- Ожиріння та інфекція гепатиту В пов'язані з підвищеним ризиком метаболічного синдрому
- Небезпечні коливання рівня цукру в крові, які можуть передбачити найгірші поширені продукти харчування, такі як винуватець!
- Відхилення повідомлень прокурора За словами Достала, це був політичний жест Нового Часа
- Низькі ціни розривають пташині зв’язки для птиці - Люди - Економіка