Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
Чилійський журнал педіатрії - офіційне видання Чилійського товариства педіатрії. Revista Chilena de Pediatría отримує до публікації лише оригінальні статті з темами клінічних або експериментальних досліджень та соціальної медицини та охорони здоров’я, пов’язані з дітьми, які не були опубліковані в інших журналах. Чилійський журнал педіатрії залишає за собою права на них. Періодичність журналу - раз на два місяці. Абревіатура його назви - Rev Chil Pediatr, яку слід використовувати в бібліографіях, виносках, легендах та бібліографічних посиланнях.
Індексується у:
Pubmed, Scielo, Scopus
Слідкуй за нами на:
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Вступ
- Визначення
- Етіологія
- Класифікація
- Чи існують різні типи гіперфенілаланінемії? Чи всі вони рівні за суворістю?
- Патофізіологія
- Клінічна картина
- Яка клінічна картина гіперфенілаланінемії?
- Діагностика
- Чому рання діагностика так важлива?
- Як проходить процедура скринінгу?
- Що пропонує чилійська програма моніторингу для ПКУ?
- Лікування
- Як можна забезпечити харчові потреби цих пацієнтів за допомогою такої обмеженої дієти?
- Яку дієту слід вказувати між підозрою та діагностичним підтвердженням?
- Що станеться, якщо пацієнт або його батьки не дотримуються дієтичних вказівок?
- Що робити, якщо зробити щеплення?
- Що робити, якщо пку дитина захворіла?
- Чи може пацієнт з гіперфенілаланінемією отримувати будь-які ліки?
- Що робити перед операцією?
- Що таке материнський синдром pku?
- Завершення
- Конфлікт інтересів
- Бібліографія
Гіперфенілаланінемії визначаються рівнем фенілаланіну в крові понад 2 мг/дл. Основною причиною є мутація гена, що кодує фенілаланінгідроксилазу, яка каталізує реакцію, яка перетворює фенілаланін в тирозин. Гіперфенілаланінемії класифікуються як доброякісні або легкі, а фенілкетонурія - легкі, помірні та класичні. Оскільки виявлення його після неонатального періоду спричиняє серйозну розумову відсталість, з 1992 року в Чилі його виявлення разом із виявленням вродженого гіпотиреозу є частиною Національної програми скринінгу новонароджених. Ця стаття має на меті відповісти на найпоширеніші запитання, які може задати педіатр, зіткнувшись з пацієнтом із гіперфенілаланінемією.
Гіперфенілаланінемії визначаються фенілаланіном крові понад 2 мг/дл. Основна причина зумовлена мутацією гена, який кодує фенілаланінгідроксилазу, яка каталізує реакцію, що перетворює фенілаланін у тирозин. Гіперфенілаланінемії класифікуються на доброякісні або легкі гіперфенілаланінемії або легкі, помірні або класичні фенілкетонурії. Через затримку виявлення поза періодом новонародженості він спричиняє важку розумову відсталість. Його виявлення разом із вродженим гіпотиреозом є частиною Національної програми скринінгу новонароджених з 1992 року в Чилі. Ця стаття має на меті відповісти на найпоширеніші запитання педіатра при зіткненні з пацієнтом із гіперфенілаланінемією.
Гіперфенілаланінемії (HFA) визначаються вмістом у крові незамінної амінокислоти фенілаланіну (FA), що перевищує 2 мг/дл.
У 1984 році в Чилі було розпочато пілотний план скринінгу новонароджених HFA, який показав, що здійснити його можливо. У 1992 році Міністерство охорони здоров'я розпочало Національну програму скринінгу на ВГС та вроджений гіпотиреоз, яка розповсюдилася на всю країну в 1996 році. В даний час вона охоплює 98,7% усіх новонароджених (НБ), встановлюючи захворюваність на класичну фенілкетонурію 1: 18 916 РН, діагностується на 18,6 ± 9 днів 1. Для HFA захворюваність становить 1: 10 198 РН. З 2005 року цей іспит є обов'язковим (Закон 19.966 про чіткі гарантії здоров'я) 1 .
Харчове лікування слід розпочинати негайно до 30 днів життя, щоб запобігти розумовій відсталості, і воно повинно підтримуватися протягом усього життя, що полягає у обмеженні амінокислоти FA з раціону та вживанні спеціальної суміші, що субсидується Міністерством охорони здоров'я до 18 років.
Мета цієї статті - відповісти на запитання, які може задати педіатр, зіткнувшись з дитиною, якій у щоденній практиці діагностовано СНВ.
HFA відповідають набору умов, що характеризуються підвищенням вмісту амінокислоти FA в крові, що визначається величиною> 2 мг/дл, і визначаються співвідношенням між амінокислотами FA і тирозином (IRR), постійно більшим за 3, використовуючи це значення в діагностичному підтвердженні 2 .
HFAs - це аутосомно-рецесивні спадкові генетичні умови, коли обох батьків вважають носіями. Ризик рецидиву захворювання становить 25% при наступній вагітності. Приблизно в 98% випадків HFA продукуються через дефіцит або відсутність ферменту гідроксилази FA, кодованого в гені 12q22-q24.1, який каталізує реакцію FA на TIR. У 1-2% випадків причиною є дефект системи кофакторів цього ферменту, тетрагідробіоптерин 3,4 .
Класифікація Чи існують різні типи гіперфенілаланінемії? Чи всі вони рівні за суворістю?
У межах HFA існують різні ступені тяжкості, явище, обумовлене великою кількістю мутацій, які різним чином впливають на активність ферменту гідроксилази FA. Ось як HFA можна класифікувати за рівнем FA плазми, толерантністю до прийому цієї амінокислоти, залишковою ферментативною активністю та мутаціями, що її породжують, на 5:
-
•
Класична фенілкетонурія (ФКУ) (OMIM 261600)
Це найважче, що визначається рівнем ФК у плазмі понад 20 мг/дл, з ВСД менше 2 мг/дл, фенілкетонами в сечі, активністю гідроксилази ФА менше 1% та толерантністю до прийому ФА менше 20 мг/дл. кг/день (від 250 до 350 мг/день).
Вони мають ФП у плазмі від 6 до 19 мг/дл, нормальний ВСД, активність АФ гідроксилази від 3 до 50% і толерантність до прийому ФА між 20-25 мг/кг/день (350-400 мг/день).
З рівнями від 4 до 6 мг/дл, толерантність до більш високого споживання ФА, від 25 до 50 мг/кг/день (400-600 мг/день).
Вони мають рівні ФА у плазмі від 2 до 4 мг/дл і нормальний рівень ВСД, активність ФА гідроксилази 50%. Він може нормалізувати рівень через 6 місяців, рекомендуючи нормальну дієту з регулярним контролем рівня.
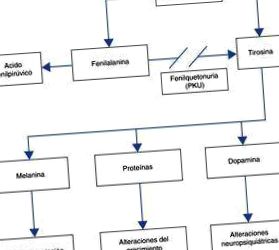
Через недостатню активність ферменту FA гідроксилази відбувається накопичення FA і, як наслідок, зменшення продукції амінокислоти TIR (рис. 1).
Патофізіологія фенілкетонурії.
Збільшення ФА в крові спричиняє конкурентне інгібування транспорту інших амінокислот через клітинні мембрани, включаючи проходження крізь гематоенцефалічний бар'єр, додатково збільшуючи концентрацію ФА в мозку. Це зменшує внутрішньонейронні концентрації амінокислот, а також конкурентно інгібує МДП та гідроксилювання триптофану, викликаючи зменшення синтезу білка з порушенням дендритної проліферації, мієлінізації та пригнічуючи синтез серотоніну, дофаміну та норадреналіну 5. З іншого боку, дефіцит ВСД пояснює вплив зростання ваги та ознаки гіпопігментації.
Клінічна картина Якою є клінічна картина гіперфенілаланінемій?
На щастя, і завдяки скринінговій програмі для новонароджених нам стає все важче знайти повну картину класичного ФКУ, як це було вперше описано в 1934 році Асбьєрном Фоллінгом, в якому діти без лікування починали в перші місяці життя нецікавість до навколишнього середовища, судоми (часто масивні спазми), екзема, яка не піддається лікуванню, і затхлий запах. У випадках, які не піддаються негайному лікуванню, затримка розвитку стає очевидною у другому триместрі життя, а потім на дошкільних та шкільних етапах серйозні порушення поведінки, агресивність, гіперактивність, самозашкодження та аутичні риси. У дорослих спостерігалася глибока розумова відсталість та судоми, важкі для лікування 5 .
В наш час, після створення скринінгової програми, діти ФКУ з хорошим метаболічним контролем не відрізняються від тих, хто не проявляє захворювання як інтелектуально, антропометрично, так і психосоціально.
Пацієнти з легким або доброякісним АФГ класифікуються як безсимптомні незалежно від контролю, однак дослідження, проведені протягом останніх десятиліть, встановили, що пацієнти з АФГ та поганим метаболічним контролем мають когнітивні зміни в нейропсихологічних дослідженнях 6,8 .
Діагноз можна поставити за допомогою краплі крові, взятої на фільтрувальному папері, яка за допомогою техніки флюорометрії здатна визначити кількість рівнів ФА в крові - метод, який використовується для проведення скринінгу новонароджених. Тандемна мас-спектрометрія (ацилкарнітиновий профіль) використовується для вимірювання співвідношення FA/TIR та підтвердження діагнозу, якщо воно становить> 3 мг/дл.
Чому рання діагностика так важлива?
Класичний ФКУ призводить до глибокої розумової відсталості, якщо його не діагностують та не лікують з періоду новонародженості. Рання діагностика до місяця життя та своєчасне введення лікування дозволяють запобігти розумовій відсталості та всім описаним наслідкам.
Як проходить процедура розслідування?
У всіх НБ, як в чилійській державній, так і в приватній системі охорони здоров’я, беруть зразок крові шляхом пункції п’ят, який відкладають на картці фільтрувального паперу, аналізуючи за допомогою модифікованої техніки флуорометрії Маккемана та Робінса. Якщо рівень ФА перевищує 2 мг/дл, він повідомляється як позитивний, і з лабораторії програми (Сантьяго чи Консепсьйон) зразок негайно просять повторити, що цього разу аналізується за допомогою тандемної мас-спектрометрії в Інституті харчування та Харчові технології (INTA) Університету Чилі, іспит, який підтверджує при визначенні рівнів FA, IRR та їх взаємозв'язку. З цим підтвердженням пацієнту призначено клінічну оцінку в INTA, де він приймається до програми.
Що пропонує чилійська програма моніторингу ФКУ?
Після підтвердження діагнозу пацієнт потрапляє до Програми моніторингу метаболічних захворювань, яка проводиться в Діагностичному центрі INTA. Чилійська держава виключно субсидує спеціальну формулу. Батьки повинні оплатити клінічні огляди та поїздки до центру направлення. Ці пацієнти повинні відвідувати регулярні огляди у дієтологів, лікарів (невропатологів або педіатрів) та з психологією згідно з попередньо встановленим графіком у програмі.
Основою лікування HFA є обмеження FA з раціону, використання вільної суміші для FA і доповнення мінералами, незамінними жирними кислотами та IRR, коли це необхідно. Спостереження є клінічним (педіатричним, неврологічним, психологічним та харчовим) та біохімічним та повинно тривати все життя. Дієта виключає всі продукти тваринного походження та продукти, отримані з них, через їх високий вміст FA, а також враховує зернові, фрукти та овочі, вміст FA яких слід ретельно розраховувати.
У виняткових випадках, у випадках легкого рівня HFA дієта може бути частково звільнена, але завжди дотримуючись суворого контролю рівня ФА у плазмі. У таблиці 1 ви можете побачити заборонені, контрольовані та дозволені продукти.
Заборонені, контрольовані та дозволені продукти при лікуванні фенілкетонурії