Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
«Шкіра» - це журнал, спрямований на постійну освіту з дерматології. З цієї причини його зацікавленість не обмежується дерматологом, а поширюється на лікарів, які починають цю спеціальність, на тих, хто виконує свої функції далеко від великих госпітальних центрів, і на лікарів-неспеціалістів, яким щодня доводиться стикатися з дерматологічними дослідженнями проблеми у щоденній практиці. Для досягнення цієї мети журнал складається з розділів: Новини, Огляди, Керівні знаки/Диференціальна діагностика, Випадки для діагностики, Шкіра в повсякденній практиці, Шкіра в контексті медицини та її спеціальностей, Дерматологічна терапія та ін. Редакційний комітет журналу забезпечує ретельність, якість, практичний інтерес та дидактичну здатність завдяки ретельному підбору тем та авторів, а також різноманітності таблиць та іконопису.
Індексується у:
Слідкуй за нами на:
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
У 1996 р. Були широко впроваджені нові комбіновані методи лікування ВІЛ-1 на основі інгібітора нуклеозидної зворотної транскриптази (NRTI), інгібітора протеази (PI) та згодом аналогів ненуклеозидних інгібіторів. Зворотна транскриптаза (NNRTI). З більш тривалим виживанням цих пацієнтів з’являється новий синдром, що характеризується перерозподілом жиру в організмі разом із порушеннями метаболізму, відомими як «ліподистрофія пацієнтів з ВІЛ» (LDHIV).
Перший описаний випадок був пов’язаний з лікуванням індинавіром у 1997 році 1; Пізніше Карр та співавт. 2 детально визначили синдром, при якому периферична ліподистрофія проявляється разом із дисліпідемією та резистентністю до інсуліну щодо лікування інгібіторами протеази.
LDHIV - це процес, який різниться за частотою та тяжкістю. Втрата периферичного жиру спостерігається переважно у деяких пацієнтів, тоді як у інших спостерігаються метаболічні зміни до того, як виявляться морфологічні зміни.
Оскільки втрата жиру відбувається поступово протягом місяців або років, раннє розпізнавання ЛДГІВ є важким, особливо у пацієнтів із ожирінням та жінок. Для виявлення змін жиру в організмі було використано кілька додаткових методів, таких як комп’ютерна томографія, магнітно-резонансна томографія, ультрасонографія або двоенергетична рентгенівська абсорбціометрія (DEXA), хоча жоден з них не є загальновизнаним.
Якщо до всього цього додати відсутність встановлених діагностичних критеріїв або відсутність консенсусних додаткових тестів, не дивно, що поширеність ЛДГІВ є настільки мінливою (від 8 до 84% із середнім значенням 42%) 3. Захворюваність зростає із збільшенням тривалості антиретровірусного лікування. Що стосується локалізації, то найчастіше уражається особа (45%), за нею йдуть кінцівки (42%), живіт (39%), руки (39%), сідниці (36%) і спинно-цервікальна область (4%) 4 .
Перерозподіл жиру в організмі
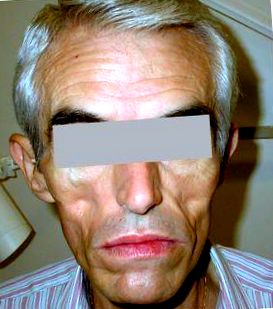
Спостерігається симетрична втрата жирової тканини з обличчя (рис. 1) та кінцівок. Постраждалі пацієнти приймають хибну мускулисту атлетичну зовнішність та характерне трупне обличчя. У деяких пацієнтів ця втрата жиру збігається з накопиченням жирової тканини навколо шиї, у тильно-шийному відділі хребта («горб буйволів») (рис. 2), у верхній частині тулуба та внутрішньочеревній області 5. Вісцеральний жир збільшується, тим самим підтримуючи запас жиру в організмі у відповідь на спостережувані метаболічні зміни.
Малюнок 1. Ліпоатрофія на обличчі.
Рисунок 2. «Горби буйволів».
Зростання грудей спостерігався у деяких пацієнток, особливо у жінок, хоча незрозуміло, чи відбувається це за рахунок жирової або залозистої тканини.
Ця фенотипова зміна є важливою фізичною стигмою для цих пацієнтів і може зменшити терапевтичну прихильність 6 .
Жирова тканина, яку класично розглядають як запас енергії, виконує складні ендокринні, метаболічні та імунні функції. Адипоцит - єдина клітина, спеціально пристосована для накопичення великої кількості жирних кислот у формі триацилгліцерину (ТГ). Інші тканини мають інші механізми регулювання надлишку жирних кислот. Печінка здатна перетворювати TG у ліпопротеїни дуже низької щільності (ЛПНЩ), а м’язи зменшують вміст ліпідів, збільшуючи м’язову активність. Натомість підшлункова залоза має лише компенсаторне бета-окислення, і, отже, вона більш вразлива до ліпоапоптозу через надлишок жирних кислот, що пояснює появу діабету у пацієнтів із ожирінням 7 .
За відсутності адипоцитів, як і при ліподистрофіях, невеликі калорійні надлишки викликають відкладення ТГ у нежирових тканинах з наслідком стеатозу печінки, інсулінорезистентності, інсуліннезалежного цукрового діабету та різного ступеня кардіоміопатії.
У 50-70% пацієнтів, які отримують інгібітори протеази, розвивається дисліпідемія, тоді як гіперглікемія спостерігається у приблизно 20% пацієнтів, які проходять лікування інгібіторами протеази, але 62% мають толерантність до глюкози 8 .
14% пацієнтів, які отримували НІЗТ, мають гіперглікемію, а 7% - цукровий діабет.
«Горб буйволів» у пацієнтів з LDHIV більше пов’язаний з гіперінсулінемією, ніж з дисліпідемією 9 .
Метаболічні ефекти, вторинні після антиретровірусного лікування, такі як дисліпідемія та резистентність до інсуліну, збільшують ураження ендотелію та сприяють розвитку проатеросклеротичного стану 10,11. Тому слід уникати інших факторів ризику, таких як тютюн, контролювати гіпертонію та сприяти фізичним вправам та правильному харчуванню.
ФАКТОРИ РИЗИКУ ЛДГІВ
Інгібітори протеази
Зовнішній вигляд LDHIV був описаний у поєднанні з усіма інгібіторами протеази, особливо індинавіром, ритонавіром та саквінавіром. Сукупна ймовірність LDHIV оцінюється у 3,2% через 6 місяців лікування, 10,7% через 12 місяців, 62,5% через 24 місяці та 75% через 30 місяців. .
Нуклеозидні інгібітори зворотної транскриптази
Як ламівудин (3TC), так і ставудин (d4T) були пов’язані з ненормальним перерозподілом жиру в організмі, який не відрізняється від такого, що спостерігається у пацієнтів з інгібіторами протеази. Однак ці пацієнти також повідомляють про втрату ваги, втому, нудоту, гепатомегалію, дисфункцію печінки та високі концентрації молочної кислоти, типові для порушеної функції мітохондрій12. .
ВІЛ-інфекція
Розвиток та тяжкість ЛДГІВ безпосередньо залежать від тривалості ВІЛ-інфекції. Тяжкість інфекції, що визначається низьким рівнем CD4, пов'язана з появою ліпоатрофії 13. Ранній початок високоактивної антиретровірусної терапії (ВААРТ) на менш запущених стадіях захворювання може мінімізувати ризик розвитку ЛДГІВ.
Харчовий статус, вік, стать та раса
У пацієнтів із надмірною вагою до прийому ВААРТ з інгібіторами протеази частіше спостерігається буйволиний горб та збільшення грудей, але менша частота липоатрофії обличчя та сідниць у порівнянні з пацієнтами із надмірною вагою. З іншого боку, низька вага перед початком лікування визначає більш важку ліподистрофію 14 .
Пацієнти старшого віку, як правило, мають більшу масу жиру в організмі, що може модулювати зміни перерозподілу жиру, що спостерігаються при LDHIV. Навпаки, зв'язок між віком та LDHIV може бути опосередкованою більшою кількістю делецій мітохондріальної ДНК (mtDNA), які відбуваються природним чином із старінням .
Жінки з ЛДГІВ набувають фенотипу андроїдів з талією: співвідношення стегон більше схоже на співвідношення чоловіків, що пов'язано з гіперінсулінемією, гіперандрогенемією, підвищеним тестостероном і співвідношенням лютропін: фолітропін та гіперліпідемією 16 .
Білі страждають на вищий ризик розвитку ЛДГІВ, ніж афроамериканці 17 .
ПАТОГЕНЕЗ ЛДГІВ
Для LDVIH було запропоновано кілька патогенних теорій, хоча найбільш широко прийнятою є мітохондріальна токсичність. NRTI - це похідні аденозину, гістидину, гуанозину та тимідину, які забезпечують альтернативні субстрати для полімераз. Інгібуючий ефект NRTI на полімерази більший для зворотної транскриптази ВІЛ> pol-γ ДНК> pol-β ДНК> pol-α ДНК = pol-ε ДНК 18. Реплікація мтДНК здійснюється за допомогою гамма-полімерази, тому NRTI також впливають на мтДНК.
Дефектна реплікація мтДНК може призвести до дефектної активності мітохондріальних ферментів, зміни OXPHOS, фосфорилюючого ланцюга, що збільшує вироблення лактату, що закінчується апоптозом мітохондрій (рис. 3).
Рисунок 3. Мітохондріальна токсичність NRTI, що включає зміну дихального ланцюга та виснаження мітохондріальної ДНК.
Здатність впливати на мітохондріальну гамма-ДНК-полімеразу більша за зальцитабін> диданозин> ставудин> ламівудин> тенофовір> зидовудин> абакавір 19 .
Встановлено, що лікування NRTI пов’язане з виснаженням мтДНК в адипоцитах, виміряне кількісною ПЛР. Середнє виснаження зидовудину становить 52,1%, тоді як для ставудину - 87,1% 20 .
ЦИТОКІНИ, АДИПОЦИНИ І ЛДГІВ
Концентрації плазми або експресія генів різних адипокінів змінюються при LDHIV. Збільшення плазми прозапальних цитокінів та зміна експресії та/або продукування адипокінів жировою тканиною може мати вирішальне значення для реконструкції жиру та метаболічних змін у цих пацієнтів. Жир у пацієнтів, які не отримували антиретровірусні препарати, свідчить про зміну експресії генів адипокінів лептину та адипонектину, а також тих, хто бере участь у диференціації адипоцитів, метаболізмі та функції мітохондрій. Це пояснювало б, що сам ВІЛ-1 зробить перший шкідливий вплив на адипоцит, і що пізніше, із запровадженням антиретровірусного лікування, морфологічні варіації, характерні для ліподистрофічного синдрому, стануть фізично очевидними 22 .
Кількість циркулюючого адипонектину зменшується у пацієнтів із перерозподілом жиру порівняно з пацієнтами без ліподистрофії. Зв'язок між низькими концентраціями адипонектину та резистентністю до інсуліну відома, хоча неможливо визначити, чи є зазначена метаболічна зміна причиною чи наслідком зниження адипонектину 23,24 .
Місцева експресія мРНК лептину та адипонектину зменшується в жирі уражених пацієнтів, тоді як експресія мРНК фактора некрозу пухлини (TNF) альфа, інтерлейкіну (IL) 6 та IL-8 збільшується на 25,26 .
Гетерозиготні для промоторної області 238G/A TNFα частіше прогресують до LDHIV, ніж пацієнти, що не гетерозиготні, з 1,7-кратним вищим ризиком. .
Відома стимуляційна здатність 1с ізоформи SREBP-1 (білок, що зв'язує стерол-регуляторний елемент) у диференціації адипоцитів. Експресія мРНК SREBP-1c істотно знижується у пацієнтів з ЛДГІВ, що корелює зі зниженням адипогенезу та інсулінорезистентності 28 .
Інгібітори протеази (менше ампренавіру) можуть змінити дозрівання ламіна/кондиціонера, викликаючи порушення ядерної архітектури, що може спричинити ядерний вивих SREBP-1c 29 і, отже, дисфункцію адипоцитів 30,31 .
Експресія генів у збільшеному дорзоцервікальному жирі або "горбі буйволів" відрізняється від жиру в інших місцях у пацієнта з ЛДГІВ, що вказує на інший патогенетичний механізм цього локалізованого накопичення жиру 32 .
Підвищена концентрація IFNα в сироватці спостерігається у пацієнтів з ліподистрофією, з позитивною кореляцією з концентрацією холестерину, тригліцеридів, ЛПНЩ та аполіпопротеїну В 33. IFNα збільшує ліполіз за допомогою прямого механізму в жирових клітинах або опосередковано шляхом стимуляції осі гіпоталамус-гіпофіз-наднирники, збільшення концентрації кортизолу, норадреналіну та глюкагону та зменшення кліренсу тригліцеридів. В цілому, IFNα сприяє дисліпідемії, що спостерігається у пацієнтів з ЛДГІВ, і є найкращим маркером змін ліпідів у цих пацієнтів.
Хоча відновлення імунітету було запропоновано як патогенний механізм для ЛДГІВ, проспективна оцінка змін тіла у лікуваних пацієнтів показує, що втрата жиру в кінцівках відбувається після періоду найбільшого відновлення імунітету, що робить етіологію малоймовірною для відновлення імунної системи у ЛДГІВ.
Таким чином, згідно з різними доказами, інгібітори протеази більше пов'язані з накопиченням вісцерального жиру та метаболічними змінами, типовими для ліподистрофічного синдрому, тоді як НІЗТ викликають мітохондріальну токсичність і є більш важливими у розвитку периферичної втрати жиру.
Суспензія інгібіторів протеази як терапевтичної стратегії не виявилася ефективною для відновлення жиру в організмі, хоча метаболічні зміни можуть покращитися. Терапевтична заміна абакавіру пов’язана із покращенням, хоча і рідко помітним, втрати жиру 34 .
Визначення деяких антиретровірусних препаратів із більшою здатністю виробляти ліподистрофію означає, що з самого початку розглядаються різні схеми терапії, а сучасні дослідження спрямовані на розробку нових препаратів з меншим або відсутністю впливу на адипоцит.
Після встановлення ліподистрофії існує кілька варіантів наповнювачів для відновлення втрат підшкірного об’єму, пов’язаних з ВІЛ-інфекцією.
Полімолочна кислота L була схвалена в Європі з 1999 року, а Управління з контролю за продуктами та ліками (FDA) у США з 2004 року для лікування ВІЛ-асоційованої ліпоатрофії обличчя. Персистенція препарату становить 3 роки і більше, і єдиним побічним ефектом, який спостерігався під час спостереження протягом 3 років, було утворення підшкірних папул, більш відчутних, ніж видимих, у 11% випадків 35 .
Іншим широко використовуваним наповнювачем є тривимірний зшитий полімер, що належить до сімейства поліалкілімідів (Bio Alcamid ®). Це фізично стабільний продукт, який після імплантації викликає утворення постійної біологічної капсули, звідси і концепція ендопротезування. Також використовується ліпофілінг, який полягає у власній трансплантації жиру пацієнту, що інколи ускладнюється важкою ліпоатрофією деяких пацієнтів 36 .
Як медикаментозне лікування у пацієнтів із центральним ожирінням, соматотропін застосовували за своїми ліполітичними та окислювальними властивостями у дозі 4 мг/день протягом 12 тижнів. Лікування супроводжується зменшенням внутрішньочеревного внутрішньочеревного жиру, але також зменшенням жиру в кінцівках та збільшенням глюкози. Цей останній ефект є важливим обмеженням для використання соматотропіну у цих пацієнтів, оскільки це погіршить резистентність до інсуліну 37 .
Застосування тіазолідиндіонів, агоністів адипогенного фактора PPARγ, може бути корисним для лікування ліпоатрофії та поліпшення чутливості до інсуліну. Однак це супроводжується зниженням рівня холестерину ліпопротеїнів високої щільності та збільшенням рівня ліпопротеїдів низької щільності, що погіршує дисліпідемію, типову для ліподистрофічного синдрому 38 .
Хоча в ліподистрофії, пов'язаній з ВІЛ-1, запропоновано безліч патогенетичних механізмів, багато невідомих залишається в патогенезі цього своєрідного розподілу жиру в організмі та у появі метаболічних порушень. Можливо, численні генетичні та вірусологічні фактори, масове вироблення цитокінів, спричинене самою інфекцією та/або відновленням імунітету та ефект різних антиретровірусних методів лікування, спільно втручаються у розвиток цього ліподистрофічного синдрому.