реферат
Головний
Завдяки покращенню виживаності після ІМТ при апластичній анемії або лімфогематологічних злоякісних захворюваннях, зростає проблема щодо консультування щодо подальшого стану фертильності. Крім того, запровадження нових режимів кондиціонування може мати різний вплив на репродукцію чоловіків. Хоча кріоконсервація сперми завжди повинна бути розроблена перед початком будь-якого цитотоксичного лікування, дуже часто ця процедура неможлива з різних причин. По-перше, коли пацієнтам, а часто і їхнім лікарям, діагностують рак у молодому віці, вони можуть не бути готовими планувати майбутні проблеми з фертильністю до початку лікування. По-друге, заморожування може бути недоступне у всіх онкологічних центрах. По-третє, у деяких пацієнтів погана якість сперми через сам стан раку раніше вважалася непридатною для заморожування до впровадження інтрацитоплазматичної ін’єкції сперми (ICSI), нової методики, яка дозволяє запліднення in vitro із невеликою кількістю сперми. Метою цього дослідження була оцінка ступеня, якості та кінетики відновлення сперматогенезу у 64 пацієнтів, які отримували різні мієлоаблативні схеми.
Пацієнти та методи
У грудні 2000 року були переглянуті клінічні карти 64 чоловіків, які пройшли алогенну ІМТ у 1982-1996 роках у відділенні гематології лікарні Сан-Мартіно в Генуї, Італія, де було проведено принаймні один аналіз сперми після лікування.
Для кожного пацієнта були отримані тип злоякісності, попередня хіміотерапія, режим кондиціонування, вік БМТ та попередній репродуктивний анамнез, а також моніторинг фертильності. Більшість аналізів сперми проводили в андрологічній лабораторії кафедри акушерства та гінекології Генуезького університету. Зразки сперми брали мастурбацією через 3 дні сексуального утримання. Аналіз сперми складався з оцінки обсягу сперми, її рухливості та кількості сперми стандартними методами згідно з наступними протоколами ВООЗ. 1 Пацієнтів вважали азооспермічними, коли в зразку в будь-якому полі двокамерного гемацитометра (Neubauer Improved) до і після центрифугування не було виявлено сперматозоїдів. Коли сперму виявляли лише після центрифугування, пацієнтів вважали криптоспермічними. Важка олігозооспермія була визначена, коли кількість сперми становила 20 × 106/мл. Рухливість сперми оцінювали за простою системою класифікації згідно з протоколом ВООЗ. 1 Морфологію сперми оцінювали на забарвлених предметних стеклах (фарбування Папаніколау) за допомогою лінзи із 100-кратним зануренням у світле поле та 10-кратним окуляром ока (Leitz), коли для дослідження було доступно принаймні 200 сперматозоїдів.
Всі зібрані дані оцінювали за допомогою комп’ютерної системи та аналізували за допомогою SAS (випуск V8, SAS Institute, Cary, NC, USA). Для категорій використовували хі-квадрат або точні тести Фішера, а для кількісних змінних - загальну лінійну модель (GLM). Кореляційний аналіз також використовувався для оцінки взаємного розподілу змінних.
результат
Середній вік пацієнтів з трансплантацією становив 27,39 ± 8, 16 (9–50). Вісімнадцять пацієнтів (28%) мали одне або більше дітей до введення БМТ. Лише 8 з них мали аналіз сперми до ВМТ, і серед них 75% показали нормозооспермічні параметри.
Показаннями до ВМТ були такі: важка апластична анемія (SAA, n = 11), гострий лімфолейкоз (ALL, n = 7), гострий мієлолейкоз (AML, n = 25), хронічний мієлоцитарний лейкоз (CML, n = 17 ), неходжкинська лімфома (NHL, n = 3) та один випадок хвороби Ходжкіна (HD).
Схема підготовки трансплантата та результати останньої проби сперми, проведеної після ВМТ, наведені в таблиці 1. Спостереження коливається від 1 до 18 років (медіана 4 роки).
Стіл в натуральну величину
До ІМТ всі пацієнти зі злоякісними пухлинами отримували різні дози та схеми хіміотерапії. У 45 випадках можна було оцінити час, що минув після закінчення хіміотерапії та ММТ, який коливався від 1 дня до 31 місяця (в середньому 158,7 дня) і становив 100 і більше днів у 60% випадків (27 із 45 пацієнтів).,
Виникнення азооспермії після BMT
Найвища частота азооспермії після ІМТ була виявлена у пацієнтів, які отримували CY плюс TBI або TAI (85,4%). Серед пацієнтів, які отримували CY плюс BU або тіотепу, 50% залишалися азооспермічними. На відміну від цього, у 10% пацієнтів, які отримували лише CY, була азооспермія. Єдиний пацієнт, підготовлений із СН, який не виявив відновлення сперматогенезу, мав останній зразок сперми лише через 2 роки після БМТ.
Не було статистичної кореляції між віком МТМ та відновленням сперматогенезу.
Якість регенерації сперматогенезу
У пацієнтів, які досягли певного ступеня сперматогенезу (табл. 2), нормозооспермія, визначена критеріями ВООЗ, спостерігалась у восьми пацієнтів після кондиціонування CY та у одного пацієнта (CVi) після CY плюс TBI.
Стіл в натуральну величину
Кінетика регенерації сперматогенезу
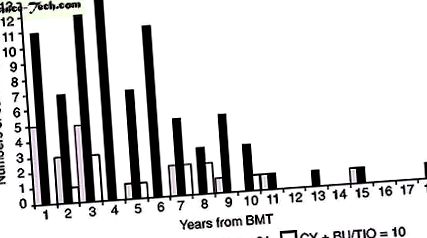
Двадцять два пацієнти мали більше одного аналізу сперми в різний час після ІМТ. Кінетику регенерації сперматогенезу неможливо статистично проаналізувати через нерегулярний розподіл спостережень через різні інтервали часу (рис. 1 і 2). Після CY + TBI регенерація сперматогенезу не спостерігалася до 4 років після трансплантації, а у двох випадках це було продемонстровано через 6 та 8 років згідно з азооспермними зразками. За режимом кондиціонування CY відновлення сперматогенезу спостерігалось у 60% пацієнтів, які пройшли обстеження через 1 рік після трансплантації.
Кількість спостережень (зразки сперми) з різними інтервалами часу від BMT відповідно до режиму кондиціонування.
Повнорозмірне зображення
Відновлення сперматогенезу після ІМТ (відсоток пацієнтів) відповідно до режиму кондиціонування.
Повнорозмірне зображення
Батьківство після БМТ
Шість пацієнтів спонтанно після ІМТ (таблиця 2). Генетичних дефектів та вад розвитку серед семи народжених дітей не зареєстровано.
обговорення
Незважаючи на те, що після ВМТ повідомлялося про вагітність, у більшості випадків батьківство не перевірялося, і зачаття, особливо за схем лікування ЧМТ, можна вважати епізодичним явищем. 2, 3, 4, 5, 6 Крім того, хоча частота вроджених аномалій, зафіксованих у живонароджених, спонтанно зачатих після лікування лімфогематологічних злоякісних захворювань, порівнянна з такою, що спостерігається серед загальної популяції, 2 можливі довгострокові генетичні пошкодження сперми не можуть бути виключено. Багато досліджень на тваринах досліджували можливі несприятливі наслідки опромінення та хіміотерапії на потомство оброблених самців. Перехідне збільшення анеуплоїдії сперми протягом 100 днів після хіміотерапії було зафіксовано у людей 9, 10, 11 .
Виходячи з цих аргументів, банку сперми слід надавати всім пацієнтам чоловічої статі, які перенесли ІМТ до будь-якого лікування, навіть якщо сперматогенез вже порушений через лімфогематологічну злоякісну пухлину. Насправді інтрацитоплазматична ін’єкція сперми (ICSI) збільшила шанси лікування чоловіків із поганим рівнем сперми та на будь-якій пробі, де навіть випадкові сперми можна виявити, що зараз вважається придатною для банківської діяльності. 12, 13
Ще одне питання, яке потрібно розглянути в цій дискусії, - чи можна створити банку сперми для пацієнтів, які вже розпочали хіміотерапію, якби не раніше. Для вирішення цієї проблеми ми проаналізували зразки сперми, відібрані до ІМТ у 30 пацієнтів з тими ж характеристиками та захворюваннями, що і досліджувана популяція, яка проходила різні схеми хіміотерапії. Переважна більшість цих пацієнтів мали б мінімальні критерії кріоконсервації сперми, лише 5 (16,6%) пацієнтів мали азооспермічний.
Хоча це можливо у більшості пацієнтів, банку сперми (1) на цьому етапі може бути відхилено (1) на основі даних тварин, що свідчать про генетичні пошкодження потомства; (2) дозволено лише в тому випадку, якщо минуло 100 або більше днів (60% випадків у цьому дослідженні) з моменту закінчення хіміотерапії, заснованої на високій частоті анеуплоїдії у спермі людини; (3) дозволено в будь-який час після інформування пацієнта до кріоконсервації, що він не зможе використовувати зразок, якщо будуть доступні нові дані про негативні довгострокові генетичні ефекти хіміотерапії на сперму.
Негативний вплив найбільш часто використовуваного режиму кондиціонування (CY + TBI) на алогенну ВМТ на кількість сперми було продемонстровано близько 20 років тому. 14 Сандерс та ін. 14 оцінювали функцію статевих залоз через 1-11 років після ВМТ та повідомляли про сперматогенез у 10 з 15 чоловіків, які отримували ІГ, і лише у двох із 32 чоловіків, які отримували ІГ плюс ЧМТ. Жодних основних даних про дослідження сперматогенезу після ВМТ не було опубліковано після дослідження Сандерса. Jacob та співавт. 15 повідомили про 42 пацієнтів, яким зробили алогенну або аутологічну ТМТ або трансплантацію периферичних стовбурових клітин, хоча зразки сперми отримали лише у 25 пацієнтів. Нещодавня публікація, що оцінювала вплив режиму кондиціонування бусульфану та циклофосфаміду на ВМТ, повідомила про виявлення сперматозоїдів у 21 з 26 досліджених чоловіків, медіана 5 років після трансплантації. 16
Це дослідження, в якому повідомляється про результати 99 зразків сперми, отриманих після ІМТ у 64 пацієнтів, надає додаткову інформацію для підтримки консультування пацієнтів та необхідність планувати більш точні терміни подальшого аналізу сперми у цих пацієнтів.
Частота азооспермії після ЧМТ може бути завищена через тривалість спостереження. У цьому дослідженні відновлення сперматогенезу відбулося лише через 9 років після трансплантації у пацієнта, який був азооспермічним 1 роком раніше. З іншого боку, 22 пацієнти (45,8%) були класифіковані як азооспермічні на основі зразка сперми, отриманого до або до 4 року після трансплантації. Кількість випадків CY-BU або CY-тіо недостатньо велика, щоб зробити висновки. Тенденція до вищої швидкості відновлення сперматогенезу, що спостерігається після цих схем, порівняно з CY-TBI (P = 0,069), якщо підтвердиться в більш масштабних дослідженнях, сприятиме вибору BU або тіотепи для кондиціонування молодих чоловіків. При режимі кондиціонування CY сперматогенез зберігається в більшості випадків (90%).
На сьогоднішній день було показано, що регенерація статевих залоз у жінок залежить від віку та менархічного статусу на момент ВМТ. У цьому дослідженні чоловічий вік при трансплантації не корелював з регенерацією сперматогенезу.
Ми не можемо зробити остаточних висновків щодо кінетики відновлення сперматогенезу після ІМТ через ретроспективний характер дослідження, який не дозволив записати всі зразки, необхідні для статистичного аналізу. Однак, виходячи з нашого досвіду, ми пропонуємо проводити тестування пацієнтів, які перебувають на CY, через 1 рік після трансплантації, тоді як після ЧМТ пацієнти не повинні проходити тестування до 4 років після BMT. Крім того, після ЧМТ важливо продовжувати спостереження протягом більш тривалого періоду (навіть 9-10 років), перш ніж робити висновки про стан фертильності пацієнта.
- Алогенна або аутологічна трансплантація кісткового мозку (bmt) для результатів неходжкинської лімфоми (nhl)
- АНАЛІЗ ТИЖНЯ Підтримка сім'ї не повинна полягати лише у збільшенні виплат
- Аналіз крові та калу на лямблії у дітей та дорослих, як це зробити Про здоров’я на iLive
- АНАЛІЗ J
- Як допомогти лікарні - Ľubovnianska nemocnica, n