Перегляньте статті та зміст, опубліковані в цьому носії, а також електронні зведення наукових журналів на момент публікації
Будьте в курсі завжди, завдяки попередженням та новинам
Доступ до ексклюзивних рекламних акцій на підписки, запуски та акредитовані курси
Місія гастроентерології та гепатології полягає у висвітленні широкого кола тем, пов’язаних з гастроентерологією та гепатологією, включаючи найновіші досягнення у патології травного тракту, запальних захворюваннях кишечника, печінки, підшлункової залози та жовчних шляхів, будучи незамінним інструментом для гастроентерологів, гепатологи, хірурги, терапевти та лікарі загальної практики, пропонуючи вичерпні огляди та оновлення на спеціальні теми.
На додаток до ретельно відібраних рукописів із систематичним зовнішнім науковим оглядом, які публікуються в розділах дослідження (наукові статті, наукові листи, редакційні статті та листи до редактора), журнал також публікує клінічні рекомендації та консенсусні документи основних товариств. . Це офіційний журнал Іспанської асоціації гастроентерології (AEG), Іспанської асоціації з вивчення печінки (AEEH) та Іспанської робочої групи з питань хвороби Крона та виразкового коліту (GETECCU). Публікація включена в Medline/Pubmed, в Індексі наукових цитат розширено, а в SCOPUS.
Індексується у:
SCIE/Journal of Citation Reports, Index Medicus/Medline, Excerpta Medica/EMBASE, SCOPUS, CANCERLIT, IBECS
Слідкуй за нами на:
Фактор впливу вимірює середню кількість цитат, отриманих за рік за твори, опубліковані у виданні протягом попередніх двох років.
CiteScore вимірює середню кількість цитат, отриманих за опубліковану статтю. Читати далі
SJR - це престижна метрика, заснована на ідеї, що всі цитати не рівні. SJR використовує алгоритм, подібний до рейтингу сторінок Google; є кількісним та якісним показником впливу публікації.
SNIP дозволяє порівняти вплив журналів з різних предметних областей, виправляючи відмінності у ймовірності цитування, які існують між журналами різних тем.
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Резюме
- Ключові слова
- Анотація
- Ключові слова
- Бібліографія
Біль у животі є найпоширенішим симптомом у пацієнтів з хронічним панкреатитом. 70–90% пацієнтів відчувають це у певний момент перебігу хвороби; у пацієнтів з алкогольним панкреатитом це зазвичай трапляється на початку, у пацієнтів з ідіопатичним панкреатитом існує форма раннього початку (юнацька), при якій біль виникає в початковій фазі захворювання, і форма пізнього початку (старечий), при якому біль проявляється пізно або може ніколи не з’явитися. За даними різних авторів, від 27 до 67% пацієнтів потребують хірургічного лікування через відсутність реакції на лікування, а також відомо, що біль може повторюватися у більш ніж 30% прооперованих пацієнтів, тому нерідкі повторні втручання . Сьогодні у нас є кілька можливостей лікування (медичне, ендоскопічне або хірургічне), і важливо індивідуально підібрати найбільш підходящий метод для кожного пацієнта.
Біль у животі є найпоширенішим симптомом у пацієнтів з хронічним панкреатитом. Від 70 до 90% пацієнтів відчувають біль у певний момент перебігу хвороби. У пацієнтів з алкогольним панкреатитом біль зазвичай відчувається при появі захворювання. Можна виділити дві різні форми ідіопатичного хронічного панкреатиту: при ранньому (ювенільному) ідіопатичному хронічному панкреатиті біль виникає спочатку, тоді як при пізньому (старечому) ідіопатичному хронічному панкреатиті біль затримується або може взагалі бути відсутнім.
За даними кількох авторів, від 27 до 67% пацієнтів потребують хірургічного втручання через відсутність реакції на лікування. Біль може повторюватися у більш ніж 30% пацієнтів, які перенесли операцію, і, отже, повторне втручання не рідкість. В даний час доступно кілька варіантів лікування: медичне, ендоскопічне та хірургічне. Найбільш відповідне лікування для кожного пацієнта слід вибирати індивідуально.
Існує дві типові схеми болю, описані Амманом: тип А у вигляді повторних загострень панкреатиту з безболісними інтервалами та тип В, що характеризується тривалими періодами постійного болю із загостреннями та, як правило, пов’язаний із ускладненнями панкреатит 1. Біль може бути слабким, помірним або сильним, може знадобитися багаторазова госпіталізація; вона зменшується в інтенсивності та частоті з часом еволюції хвороби і може навіть спонтанно зникнути, але ми не маємо прогнозуючих факторів на той момент. Це біль, що часто виникає при прийомі всередину, саме тому він, як правило, пов’язаний із втратою ваги.
Етіологія болю недостатньо добре встановлена і може бути багатофакторною, 3 але вже визнано низку факторів, які можуть сприяти її розвитку та підтримці. Серед них виділяються:
-
1.
Підвищення внутрішньопротокового та паренхіматозного тиску спричиняє синдром компартменту, що індукує ішемію, що було продемонстровано різними експериментальними дослідженнями. Як правило, цей тип болю добре реагує на ендоскопічний або хірургічний дренаж.
Зміни нейронів, такі як збільшення кількості нейронів та їх гіпертрофія (явище, також описане пізніше при раку підшлункової залози) 5. Показана позитивна кореляція між ступенем інфільтрації підшлункових нервів імунними клітинами та пластичністю нейронів (виміряна за GAP-43) з інтенсивністю болю 6 .
Постійність прийому алкоголю. Відомо, що алкоголь є дуже важливим фактором у виробництві дисфункції підшлункової залози та болю у пацієнтів з алкогольним панкреатитом. У пацієнтів, які продовжують утримуватися, погіршення функції підшлункової залози відбувається повільніше, а реакція на лікування болю краща, ніж у пацієнтів, які підтримують споживання алкоголю 7,8. Алкоголіки, як правило, завзяті курці, і сьогодні роль тютюну в еволюції панкреатиту, незважаючи на суперечливість, становить найбільший інтерес 9,10 .
Некроз підшлункової залози з утворенням псевдокісти, який може стискати жовчну протоку, протоку Вірсунга або шлунок. У цьому випадку лікування ускладнення внутрішнім ендоскопічним дренажем, зовнішнім дренажем, керованим ультразвуком/комп’ютерною томографією (КТ), або хірургічним дренажем повністю вирішить біль.
Методи, які зазвичай використовуються для лікування болю у хворих на хронічний панкреатит:
-
1.
Майбутнє лікування: введення знеболюючих засобів (включаючи опіоїди) та антидепресантів.
Зниження внутрішньопанкреатичного тиску: придушення секреції підшлункової залози (ферменти підшлункової залози, октреотид) або усунення обструкції (розміщення протеза в Вірсунгу, видалення каменів, хірургічне шунтування).
Модифікація нервової трансмісії: блокада целіакіального сплетення, хірургічна резекція.
Зниження окисного стресу: лікування антиоксидантами та алопуринолом.
Взагалі, дуже важко оцінити ефективність лікування через різну структуру болю, супутній алкоголізм у багатьох випадках та опіоїдну залежність, яку вже мають деякі пацієнти. З цієї причини для оцінки будь-якого нового лікування дуже важливо використовувати об'єктивні методи, такі як щоденний запис споживання знеболюючих препаратів та використання візуальної аналогової шкали (в якій пацієнт може щодня представляти біль), а також використання анкети якості життя у кожному з візитів.
Медикаментозне лікування Введення знеболюючих засобів
Внаслідок природного анамнезу хронічного панкреатиту відомо, що з плином часу та прогресуванням екзокринної недостатності підшлункової залози біль може зменшуватися або зникати (гіпотеза про спалену підшлункову залозу) Для одних авторів біль зменшується або зникає у 90% пацієнтів 1, а для інших у 56–79% залежно від ідіопатичної або алкогольної етіології 2. У дослідженні Mullhaupt et al., Проведеному у хворих на алкогольний панкреатит, було виявлено, що медіана часу, що минула до припинення болю, становила 10 років (діапазон, 0-30), і у більшості пацієнтів це збігалося з початком екзокринної та ендокринна недостатність підшлункової залози. Однак інші автори вважають, що не існує взаємозв'язку між припиненням болю та недостатністю підшлункової залози 2 .
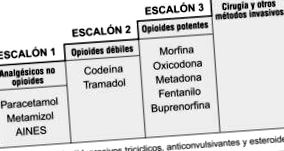
Враховуючи ці дані, коли пацієнт не реагує на незначні знеболюючі засоби (парацетамол і метамізол), протизапальні засоби (ібупрофен, кеторалак), що вводяться з антидепресантами для посилення їх дії (хоаналгетики) або слабкі опіоїди, і йому потрібно перейти до третього етапу. знеболюючої шкали Всесвітньої організації охорони здоров’я (рис. 1) протягом тривалого часу необхідно розглянути інший вид ендоскопічного або хірургічного лікування, щоб уникнути звикання до опіатів.
Знеболююча шкала при раку підшлункової залози, пристосована для лікування болю при хронічному панкреатиті. Перший крок - для легкого та помірного болю, другий - для середньо-сильного болю, а третій - для сильного болю. НПЗЗ: нестероїдні протизапальні засоби.
Ідея введення ферментів підшлункової залози для зменшення болю заснована на негативному зворотному зв’язку, який буде встановлений шляхом пригнічення секреції підшлункової залози шляхом зменшення вивільнення CCK за рахунок збільшення внутрішньодуоденального трипсину. Опубліковано 6 подвійних сліпих рандомізованих проспективних досліджень: 2 з них виявляють переваги від лікування, а інші 4 неефективні. Так само був опублікований мета-аналіз, в якому не продемонстровано значного терапевтичного ефекту із застосуванням ферментів для лікування болю 12. З цієї причини, можливо, знадобляться додаткові дослідження щодо модифікації складу препарату або визначення типу пацієнтів, які могли б отримати від нього користь, перш ніж рекомендувати його використання.
Також з метою інгібування секреції підшлункової залози були опубліковані 3 проспективні, рандомізовані та подвійні сліпі дослідження, у двох з яких використовувались різні дози, і результати були не ефективнішими, ніж при застосуванні плацебо. .
Зниження окисного стресу Антиоксиданти
Протягом останнього десятиліття було описано збільшення рівня вільних радикалів кисню в крові та секреції підшлункової залози у пацієнтів із хронічним панкреатитом. У цих пацієнтів підвищений окислювальний стрес, що призводить до збільшення вироблення вільних кисневих радикалів. Одним із факторів, які вважають причиною підвищеного окисного стресу, є відносний дефіцит антиоксидантних речовин, таких як каротини, вітамін С та Е, метіонін та селен.
Перші опубліковані дослідження з антиоксидантами використовували один антиоксидант для лікування болю при хронічному панкреатиті і показали незначну ефективність препарату, але два дослідження, опубліковані пізніше, в яких використовували сполуку з декількох антиоксидантів (метіонін, селен, бета-каротин, вітамін С і E) показали більшу ефективність, зменшуючи біль та покращуючи якість життя цих пацієнтів 13,14. В даний час проводиться європейське багатоцентрове дослідження у пацієнтів із спадковим або ідіопатичним панкреатитом, яке охопить велику кількість пацієнтів.
Опубліковано лише одне дослідження з алопуринолом, в якому його ефективність не продемонстрована 15 .
У 1964 році в медичній літературі з'явилися перші результати лікування променевої терапії для зняття болю у хворих на хронічний панкреатит. 56 пацієнтів (33 вже прооперованих і з рецидивом болю) отримували 5 Гр, а через 2 роки 37 пацієнтів все ще не мали болю 16. У 1972 році 9 пацієнтів (6 з них раніше прооперовані) отримували дози від 10 до 50 Гр, а через 2 роки 6 пацієнтів залишалися безболісними 17. Остання опублікована робота включала лікування одного пацієнта із загальною дозою 7 Гр, і він залишався безсимптомним через 3 роки після лікування 18 .
Ми провели дослідження на 15 пацієнтах (2 раніше прооперованих від болю) з використанням одноразової дози 8 Гр у пацієнтів з повторними спалахами панкреатиту та/або постійним болем. Лікування було ефективним у 13 пацієнтів, які залишались безсимптомними на 3 роки 19 .
Ми вважаємо, що це альтернатива, яку слід враховувати перед призначенням хірургічного лікування у пацієнтів, які потребують резекції.
Показання до ендоскопічного лікування підшлункової залози за останній час зросли, і це корисно при різноманітних розладах підшлункової залози, включаючи хронічний панкреатит, повторний гострий ідіопатичний панкреатит, витікання або порушення проток підшлункової залози, дренування псевдокісти та профілактику панкреатиту після ендоскопічна ретроградна холангіопанкреатографія (ERCP).
Корисність ендоскопії для лікування болю підшлункової залози визначається двома різними діями: лікування захворювання протоки Вірсунга за допомогою ендотерапії підшлункової залози та ендоскопічного блокування целіакіального сплетення під контролем ультразвуку.
Перешкода потоку підшлункової залози спричиняє підвищення внутрішньопротокового тиску, і оскільки підшлункова залоза є погано розтяжною тканиною, це підвищення тиску може спричинити підвищення тканинного тиску та ішемію. Ендоскопічне лікування, спрямоване на декомпресію закупореної протоки підшлункової залози, пов'язане зі зменшенням болю 20,21 .
У 2002 р. Rösch опублікував багатоцентрове дослідження, яке включало 1018 пацієнтів з 8 різних центрів із середнім періодом спостереження 5 років, ендоскопічно пролікованих з приводу обструкції протоки підшлункової залози внаслідок стенозу (47%), каменів (18%) або обох (32%). Пацієнтів лікували різними ендоскопічними процедурами. Наприкінці дослідження 60% пацієнтів закінчили ендоскопічне лікування, 16% все ще перебувають у процесі лікування, а 24% потребують хірургічного лікування. Зменшення болю (виміряне за допомогою структурованого опитувальника) було досягнуто у 65% пацієнтів, не відзначаючи поліпшення функції підшлункової залози 22 .
Стеноз протоки підшлункової залози є загальним проявом хронічного панкреатиту і може бути пов’язаний з каменями, псевдокістами та новоутвореннями підшлункової залози. Ендоскопічне лікування стенозу в основному показано пацієнтам з рефрактерними болями в животі, незалежно від того, чи є у них супрастенотична дилатація Вірсунга.
Численні публікації свідчать про те, що ендоскопічне встановлення стента в протоці підшлункової залози покращує постійний або періодичний біль при хронічному панкреатиті у більшості пацієнтів з технічним успіхом 72–100%, поліпшенням болю у 75–94% та підтримкою довготривалого поліпшення стану 52–74% 23–25 .
Камені підшлункової залози виявляються у 22–60% хворих на хронічний панкреатит. Камені можуть спричинити перешкоду потоку підшлункової залози з подальшим підвищенням внутрішньопротокового тиску. Для ендоскопічного лікування каменів підшлункової залози застосовується широкий спектр методів, включаючи літотрипсію та сфінктеротомію Вірсунга, разом із методами видалення каменів. Повідомлялося про значне зменшення болю при застосуванні цих методів, і це поліпшення, очевидно, пов’язане з вирішенням патологічного розширення Вірсунга. У 6 недавніх дослідженнях було включено загалом 328 пацієнтів, у яких використовувались різні ендоскопічні методики, що дозволило зменшити біль у 50–85% пацієнтів у 15–25 місяців 26–30. Це стосується конкрементів Вірсунга, і лікування конкрементів вторинних кінцівок ще не визначено.
При будь-якому ендоскопічному лікуванні існує власний ризик ускладнень, але ендотерапія підшлункової залози має особливо високий ризик. Ранні ускладнення включають панкреатит, біль, розрив Вірсунга, крововилив та холангіт, частота яких становить 15–24%. Пізні ускладнення пов'язані зі змінами паренхіми та протоки, подібними до хронічного панкреатиту, а також ускладненнями, пов'язаними з протезуванням (міграція, оклюзія) 26,31 .
Роль, яку повинні виконувати ендоскопічні методи в лікуванні хронічного панкреатиту, ще не визначена. Ці методи часто є складними і не позбавлені ускладнень, тому їх слід виконувати лише в центрах, що мають досвід у цій галузі.
Ендоскопічний невроліз чревного сплетення, керований ультразвуком
Невроліз целіакіального сплетення (PCN) - це хімічна спланіцектомія за допомогою спирту, яка викликає абляцію аферентних нервових волокон, що передають біль з черевних органів. NPC часто використовується для полегшення болю, пов’язаного з новоутвореннями підшлункової залози, а також для зменшення болю при хронічному панкреатиті.
PCN може проводитися через шкіру, хірургічним шляхом або за допомогою ендоскопічного ультразвуку. Виконання цієї методики за допомогою ендоскопічного ультразвуку (EUS) забезпечує більш прямий доступ до чревного сплетення, ніж інші методи 32. Целіакічний ганглій розташований біля початку стовбура целіакії, який легко ідентифікувати за допомогою ендоскопічного ультразвуку (рис. 2). Відносна близькість чревного ганглія до задньої стінки шлунка дозволяє безпечно вводити ганглій, мінімізуючи можливі ускладнення та потенційно збільшуючи ефективність.
- Санаторій в Женеві, Трускавець, лікування в комфорті гастроентерології
- Туберкульоз г; стрічка; переглянуто; n підпирати; сайт справи Гастроентерологія та Гепатологія
- Що таке Lida Daidaihua Ідеальне лікування для схуднення Інтернет-аптеки Іспанія - Продаж
- Що очікувати від лікування солю-медролом для РС - розглянуто
- Що робити, коли у вас болять м’язи, спричинені добавками з червоним дріжджовим рисом