Травна система - відділ внутрішньої медицини. Лікарня Санта-Барбара. Пуертольяно, Сьюдад-Реал.
КОРЕСПОНДЕНЦІЯ
Алехандро Репізо Ортега
Служба травної системи
Лікарня "Virgen de la Salud"
Авда Барбер 30, 45004 Толедо
Вступ
Кістозні ураження підшлункової залози є відносно поширеною знахідкою у пацієнтів, які проходять візуалізацію. Збільшення рівня захворюваності на ці ураження в останні роки було пов’язане з вдосконаленням та полегшенням доступу до методів візуалізації, переоцінками уражень, спочатку класифікованими як хронічний панкреатит-псевдокіста підшлункової залози, та підвищеним інтересом до цих патологій. Так, у референтних центрах третього рівня описано, що в дев'яностих роках хірургічні операції на підшлунковій залозі за цим показником становили 16% усіх резекцій підшлункової залози, тоді як в даний час вона зросла до 30% [1].
Диференціальна діагностика
Кісти підшлункової залози включають неоднорідну групу уражень з вродженим, запальним, інфекційним або пухлинним походженням. Серед кістозних пухлин є справжні кісти, такі як серозна та муцинозна цистаденома, кістозні розширення проток підшлункової залози, такі як внутрішньопротокова папілярна муцинозна неоплазія (IPMN), або кістозні ділянки некрозу в твердих пухлинах, таких як солідна псевдопапілярна пухлина, пухлинна кістозна нейроендокринна або іноді протокова аденокарцинома (табл. 1). Основною метою діагностики цих уражень буде розрізнення кістозних пухлин від непухлинних, а у пухлин - диференціація між доброякісними та злоякісними або потенційно злоякісними ураженнями.
Таблиця 1
Кістозні ураження підшлункової залози
| Псевдокіста Звичайна псевдокіста Кістозна дистрофія Псевдокіста інфекційного походження Кіста з муцинозним епітелієм Внутрішньопротокова папілярна муцинозна пухлина Муцинозна цистаденома Муцинозна цистаденокарцинома Мукоцел та ретенційні кісти Серозні кістозні пухлини Серозна цистаденома Серозна цистаденокарцинома Кісти, пов’язані з VHL Кісти з плоским епітелієм Кіста лімфоепітелію Дермоїдна кіста Кіста плоскої протоки Кісти, обмежені ацинарними клітинами Цистаденокарцинома ацинарних клітин Ацинарна клітинна цистаденома Кіста ендотелію Лімфангіома Некротичні кісти у солідних пухлинах Солідна псевдопапілярна пухлина Кістозна нейроендоскринна пухлина Протокова аденокарцинома Кістозне мезенхімальне новоутворення Інші кістозні ураження Кістозна гамартома Ендометріотична кіста Вторинні пухлини Вроджені кісти Інші кістозні ураження |
Псевдокіста підшлункової залози. Ураження запального походження, яке, як правило, вкрите неепітелізованою стінкою, що складається з фіброзної та грануляційної тканини [2], [3]. У класичних хірургічних серіях це описується як найбільш часте кістозне ураження підшлункової залози (70%). Отже, першим важливим аспектом диференціальної діагностики буде відрізнити його від інших уражень, особливо кістозних пухлин підшлункової залози. Для цього буде важливо зібрати такі дані, як наявність у техніках візуалізації запальних ознак у паренхімі підшлункової залози або відомий анамнез гострого або хронічного панкреатиту, хоча слід враховувати, що іноді ці пухлинні ураження є причиною панкреатит [1] - [6].
Серозні цистаденоми. Ці ураження становлять 30% кістозних пухлин підшлункової залози, виявлених у клінічній практиці. З гістологічної точки зору вони характеризуються тим, що їх обмежують епітелієм з однією лінією кубоїдальних клітин, багатих глікогеном. Ці пацієнти мають середній вік при діагнозі 50 років із переважанням 4: 1 серед жіночої статі і, як правило, протікають безсимптомно. Зазвичай це ураження розташоване в тілі або хвості підшлункової залози і рідше в голові. Найбільш часта форма - мікрокістозна, утворена чітко визначеною губчастою пухлиною, складеною з невеликих кіст, наповнених прозорою прозорою рідиною. Значно рідше зустрічаються макрокістозні форми. Злоякісна дегенерація серозних цистаденом підшлункової залози надзвичайно рідка, тому її слід розглядати та лікувати як доброякісне ураження [1-6].
Муцинозні цистаденоми. Він представляє 20% кістозних пухлин підшлункової залози і представляється як чітко визначене, округле ураження з товстою фіброзною капсулою, що оточує кістозні простори, які не зв’язані з протокою підшлункової залози. З гістологічної точки зору найхарактернішою знахідкою буде наявність субепітеліальної строми з клітинами веретена, які нагадують строму яєчників. У цих пацієнтів переважає жіноча стать, і вони часто протікають безсимптомно, ураження діагностується випадково під час обстеження, проведеного за іншим показанням. Коли симптоми з’являються, вони пов’язані з масовим ефектом, що призводить до великих уражень [3]. Основний інтерес у виявленні цих пухлин полягає в тому, що це потенційно злоякісне ураження, при якому можуть співіснувати різні ступені дисплазії, карциноми in situ або інвазивної карциноми. Наявність інвазивної карциноми коливається залежно від серії від 5 до 30%. Слід врахувати, що інвазивний компонент можна виявити в невеликій частині ураження, тому рекомендується гістологічний огляд всього хірургічного зразка [1] - [6].
Техніка візуалізації
Рентгенологічні дані, які зазвичай спостерігаються при псевдокістах підшлункової залози, - це наявність чітко визначеної колекції підшлункової або перипанкреатичної залози, яка іноді може спричиняти твердий або напівтвердий вміст через детрит або септації. Гострі або хронічні запальні ознаки часто спостерігаються в сусідній паренхімі підшлункової залози [7].
При серозній цистаденомі найчастіша полікістозна форма (приблизно 70%), що характеризується скупченням невеликих кіст, а іноді (15%) може спостерігатися кальцинований центральний рубець. Коли ці ураження в основному складаються з численних кіст розміром менше 1 см, у звичайних методах візуалізації це може навіть здатися твердою пухлиною [7].
У муцинозних цистаденомах найбільш частою формою прояви є макрокістозна (80%), і вона рідко буває багатоколірною. Зазвичай це ураження 4-5 см, а іноді із перегородками всередині. В інших випадках спостерігаються автентичні пухлинні маси, пов’язані з кістозним ураженням, навіть помітне вражаюче і нерегулярне потовщення стінки та кальцифікація кістозної стінки, що надає вигляду «яєчної шкаралупи». Ці дані свідчать про злоякісну дегенерацію [7].
Рентгенологічні дані, які часто зустрічаються у PCNMP, включають розширену та звивисту магістральну протоку підшлункової залози (зазвичай> 1 см у діаметрі), а іноді і кістозні розширення вторинних гілок внаслідок як вироблення муцину, так і проксимальної обструкції каналу. RC-MPN присутні на візуалізації як кістозні або мультикістозні ураження, подібні до "грона винограду" у зв'язку з нерозширеною головною протокою підшлункової залози. Кістозні ураження, пов’язані з цим видом пухлини, зазвичай невеликі, рідше> 2 см; вони частіше розташовуються в голові та перешийоку підшлункової залози, і в 39-64% випадків це мультифокальні ураження. Наявність супутньої твердої маси, вузликових або тім'яних порушень свідчить про злоякісне переродження цих уражень.
Ендоскопічні методи
Ендоскопічне ультразвукове дослідження, використовуючи високочастотний ультразвуковий промінь та уникаючи повітряних артефактів, що обмежують дослідження підшлункової залози при трансабдомінальному ультразвуковому дослідженні, дозволяє візуалізувати невеликі вогнища ураження та детально оцінити внутрішню архітектуру кіст [11] - [16].
Ендоскопічне ультразвукове дослідження корисне для характеристики стінки та вмісту псевдокіст підшлункової залози та, виходячи з цього, вибору найкращої терапевтичної процедури в кожному випадку. Багато збірників рідини підшлункової залози, розглянуті за допомогою інших методів візуалізації, можуть містити твердий або напівтвердий матеріал, який не видно на цих сканах. Спроба ендоскопічного або черезшкірного дренування цих вогнищ може бути не корисною для отримання повного дренажу та перетворення стерильної колекції в інфіковану колекцію [11] - [16] (рис. 1).
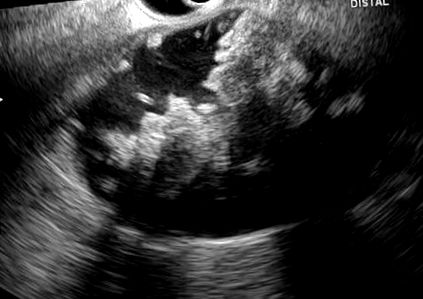
Фігура 1
Псевдокіста підшлункової залози з ехогенним матеріалом у внутрішній частині щодо детриту у пацієнта з важким гострим панкреатитом.
Іноді серозні цистаденоми можна спочатку класифікувати як тверді ураження за допомогою інших методів візуалізації. За допомогою ендоскопічного ультразвуку можна спостерігати, як ці ураження складаються з безлічі мікрокістозних уражень, що надають вигляд «стільникового» або «листкового тіста» [11] - [16] (рис. 2).
Малюнок 2
Серозна цистаденома з дрібними перегородками всередині, що сходяться в центральному рубці.
Ехоендоскопічний вигляд муцинозних ушкоджень, як правило, макрокістозний і одножильний із перегородками, які ділять його на відділи. Наявність множинних папілярних інвагінацій та пристінкових нерівностей свідчить про злоякісну дегенерацію ураження (рис. 3). Однак при муцинозних ураженнях передопераційна диференціація між доброякісними та злоякісними ураженнями, за винятком випадків масової або екстрапанкреатичної пухлинної інвазії, неможлива до проведення гістогістологічного дослідження всього хірургічного зразка [11-16].
Малюнок 3
Муцинозна цистаденома в тілі підшлункової залози.
В ІПМН ендоскопічне ультразвукове дослідження дозволяє ідентифікувати зв’язок протоки підшлункової залози з кістозними ураженнями, візуалізувати невеликі вогнища, детально оцінити внутрішню архітектуру і навіть раннє виявлення вузлів на стінці або тім’яних порушень, які не видно за допомогою інших методів візуалізації (Рисунок 4 ). Ендоскопічно відкрите папілярне отвір спостерігається у 25-40% PCMNI, через яке ідентифікується спонтанне витікання слизу.
Малюнок 4
Внутрішньопротокове папілярне муцинозне новоутворення. Кістозне ураження при спілкуванні з додатковою гілкою підшлункової залози та з ехогенним вмістом по відношенню до муцину.
Інтрацистичний аналіз рідини
У більшості випадків диференціальний діагноз кістозних уражень підшлункової залози може бути проведений на основі клінічних даних та результатів різних методів візуалізації. Але у підгрупі пацієнтів ще не буде ясно, чи є ураження псевдокістою або кістозною пухлиною, чи є це серозним або муцинозним ураженням, чи це ПМНІ, чи обструктивний хронічний панкреатит, чи навіть це серозна цистаденома або PPMN. У цих випадках корисним буде внутрішньокістозний аналіз рідини [16] - [18].
Цитологія часто не дозволяє диференціювати псевдокісти від кістозних пухлин. Цитологічний аналіз аспірату при серозних цистаденомах є діагностичним лише у 50% випадків (наявність кубоїдальних клітин із забарвленням глікогену та без муцину) та менш ніж у 50% муцинозних кіст, стовпчастого епітелію та наявності муцину. Крім того, низьке негативне прогностичне значення описується в діагностиці злоякісної дегенерації [16] - [18].
При ураженнях, що спілкуються з протокою підшлункової залози, амілаза підвищена у внутрішньокистозній рідині; як у псевдокістах, так і в MPN. У пацієнтів з добре задокументованим епізодом гострого панкреатиту, одиничним кістозним ураженням без перегородок та підвищеною внутрішньокистозною амілазою може бути поставлений діагноз псевдокісти підшлункової залози [16] - [18].
Визначення множинних онкологічних маркерів у внутрішньокістозній рідині було використано для спроби підвищити діагностичну ефективність аспіраційної пункції кісти підшлункової залози. Значення CA 19-9 у внутрішньокистозній рідині є суперечливим і, схоже, не приносить великої користі. Найбільш широко використовуваними на практиці є внутрішньокістозні значення СЕА: Збільшення понад 800 нг/мл є надійним для діагностики муцинозного ураження (чутливість 48%, специфічність 98%); тоді як значення нижче 5 нг/мл дозволяє виключити муцинозне ураження (чутливість 50%, специфічність 95%). Комбінація тестів, включаючи ендоскопічний зовнішній вигляд ультразвуку, не представляється більш точною, ніж окремі значення СЕА [16] - [18].
У клінічній практиці ситуації, коли дослідження внутрішньокістозної рідини буде особливо корисним, є у безсимптомних пацієнтів, пацієнтів з високим хірургічним ризиком та у тих, хто має стійкі мультикістозні ураження після погано або погано задокументованого епізоду гострого панкреатиту [16] - [18].
Лікування та спостереження
Малюнок 5
Класифікація кістозних уражень підшлункової залози.
БІБЛІОГРАФІЯ
Brugge WR, Lauwers GY, Sahani D, Fernández del castillo C, Warshaw AL. Кістозні новоутворення підшлункової залози. N Engl J Med 2004; 351: 1218-26.
Шейман Дж. Кістозне ураження підшлункової залози. Гастроентерологія 2005; 128: 463-9.
Sarr MG, Murr M, Smyrk TC, Yeo CJ, Fernández del Castillo C, Hawes RH, Freeny PC. Первинні кістозні новоутворення підшлункової залози: Неопластичні розлади, що мають важливе значення - питання без відповіді. J Gastrtointest Surg 2003; 7: 417-28.
Tanaka M, Chari S, Adsay V, Fernández del Castillo C, Falconi M, Shimizu M et al. Міжнародні рекомендації щодо консенсусу щодо лікування внутрішньопротокових папілярних муцинозних новоутворень та муцинозних кістозних новоутворень підшлункової залози. Панкреатологія 2006; 6: 17-32.
Khalid A, Brugge W. ACG практичні вказівки щодо діагностики та лікування новоутворених кіст підшлункової залози. Am J Gastroenterol 2007; 102: 2339-49.
Oh HC, Kim MH, Hwang CY, Lee TY, Lee SS, Seo DW et al. Кістозні ураження панкреасу: складні питання в клінічній практиці. Am J Gastroeneterol 2008; 103: 229-39.
Martínez-Noguera A, D´Onofrio M. УЗД підшлункової залози. Звичайна візуалізація. Зображення черевної порожнини 2006; 32: 136-49.
Claudon M, Cosgrove D, Albrecht T, Bolondi L, Bosio M, Calliada F et al. Рекомендації та рекомендації щодо належної клінічної практики щодо ультразвуку з посиленим контрастом (CEUS) - Оновлення 2008. Ultraschall в Med 2008; 29: 28-44.
Rickes S, Wermke W. Диференціація кістозних новоутворень підшлункової залози та псевдокіст шляхом звичайного та підсиленого відлунням ультразвуку. J Gastroenterol Hepatol 2004; 19: 761-6.
D´Onofrio M, Megibow AJ, Faccioli N, Malago R, Capelli P, et al. Порівняння контрастної сонографії та МРТ для відображення анатомічних особливостей кістозних мас підшлункової залози. AJR Am J Roentgenol 2007; 189: 1435-42.
Брюгге WR. Роль EUS у діагностиці кістозних уражень підшлункової залози. Gastrointest Endosc 2000; 52: S18-22.
Брюгге WR. Оцінка кістозних уражень підшлункової залози з EUS. Gastrointest Endosc 2004; 59: 698-707.
Koito K, Namiero T, Nagakawua T, Shyonai T, Hirokawa N, Morita K. Одиночна кістозна пухлина підшлункової залози: EUS-патологічна кореляція. Gastrointest Endosc 1997; 45: 268-76.
Sedlack R, Affi A, Vazquez-Sequeiros E, Norton ID, Clain JE, Wiersema MJ. Корисність EUS при оцінці кістозних уражень підшлункової залози. Gastrointest Endosc 2002; 56: 543-7.
Frossard JL, Amouyal O, Amouyal G, Palazzo L, Amaris J, Soldan M et al. Виконання ендосонографічної аспірації та біопсії тонкої голки під час діагностики кістозних уражень підшлункової залози. Am J Gastroenterol 2003; 98: 1516-24.
Brugge WR, Lewandrowski K, Lee-Lewandrowski E, Centeno BA, Szydlo T, Regan S et al. Діагностика кістозних новоутворень підшлункової залози: Звіт про спільне дослідження кісти підшлункової залози. Гастроентерологія 2004; 126: 1330-6.
ван дер Ваай Л.А., ван Даллемен Х.М., Порте Р.Ж. Аналіз рідини кісти в диференціальному діагнозі кістозних уражень підшлункової залози: зведений аналіз. Gastrointest Endosc 2005; 62: 383-9.
Брюгге WR. Чи слід резекувати всі кістозні ураження підшлункової залози? Аналіз кістозної рідини в диференціальній діагностиці кістозних уражень підшлункової залози: мета-аналіз. Gastrointest Endosc 2005; 62: 390-1.
Spinelli KS, Fromwiller Te, Daniel RA, Kiely JM, Nakeeb A, Komorowski RA et al. Кістозні новоутворення підшлункової залози. Спостерігати або діяти. Ann Surg 2004; 239: 651-9.
Handrich SJ, Hough DM, Fletcher JG, Sarr M.G. AJR Am J Roentgenol 2005; 184: 20-3.